مطالب مرتبط:
- معرفی تجهيزات آزمايشگاهی
- توضیح کامل تکنیک SDS-PAGE + رفع اشکال تکنیک الکتروفورز عمودی
- راهنمای کامل الکتروفورز آگارز + تصویری | بیوتکنولوژی
- رفع اشکال کامل و تخصصی الکتروفورز DNA | ژل اگارز| بیوتکنولوژی
- تئوری و مبانی کامل ژل الکتروفورز +تصویری | بیوتکنولوژی
- اصول تکنیک الکتروفورز DGGE (ژل الکتروفورز با گرادیان شیب ماده دناتوره کننده)
- تکنیک الکتروفورز دو بعدی | بیوتکنولوژی
- الکتروفورز پروتئین سرم(SPEP) | روش اجرا | و شرح کامل اجزای سرم پروتئین
- ایزوالکتروفوکوسینگ | IEF | بیوتکنولوژی | الکتروفورز با نقطه ایزوالکتریک
جداسازی بیولوژیک
فهرست مطالب
- DNA
- سانتریفوژ
- فیلتراسیون
- تخریب سلولی
- جداسازی
- رسوب دهی
- جذب سطحی
- کروماتوگرافی
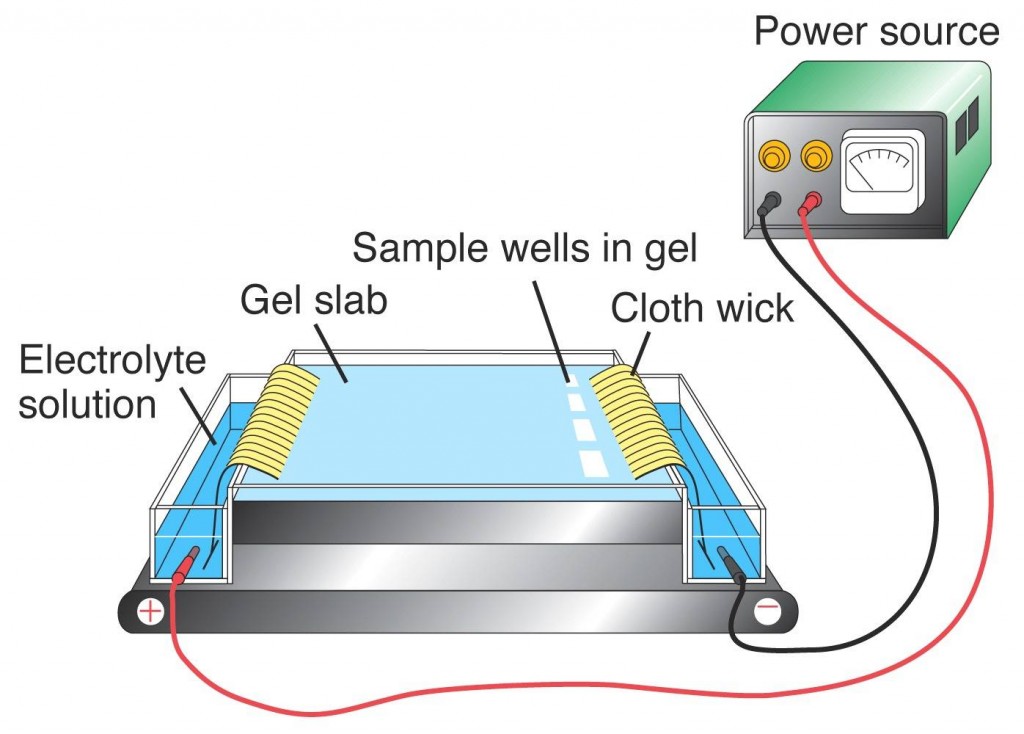
- الکتروفورز
- الکترودیالیز
- کریستالیزاسیون
- خشک کردن
- خشک کنها
فناوری DNA نوترکیب
مقدمه
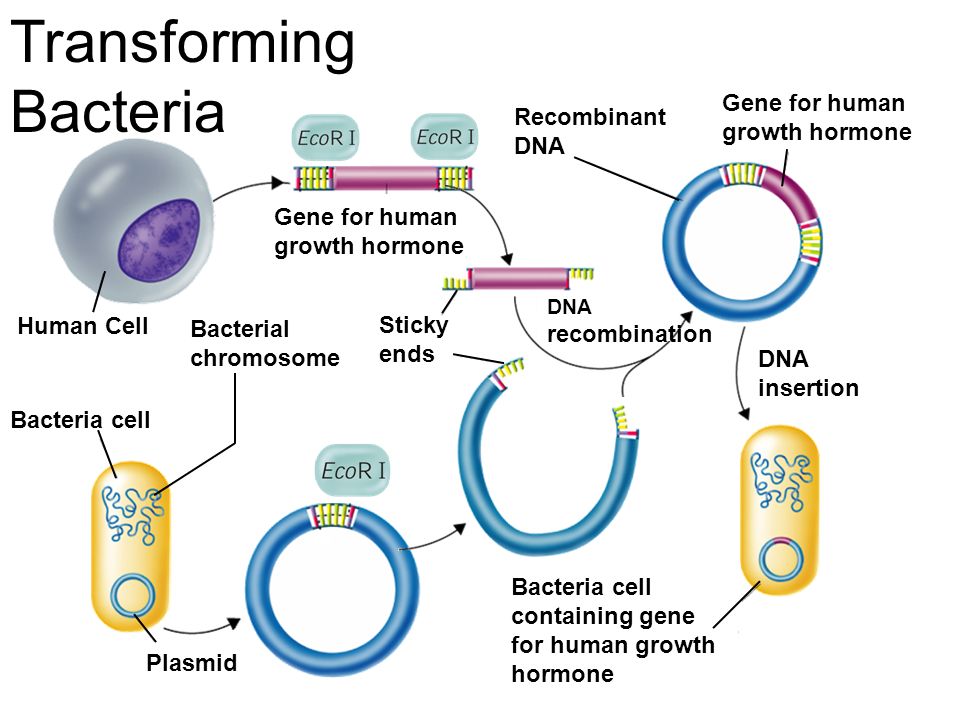
تكنولوژی DNA نوتركیب یا Recombinant DNA Technology مجموعهای از تكنیكهای مرتبط با DNA است كه با وارد شدن به عرصة دانش بیولوژی در اوایل دهة ۱۹۷۰ میلادی، انقلابی در تحقیقات علوم پایه زیستی و نیز بیوتكنولوژی به وجود آورده است. تكنیك همانند سازی ژن یا Gene Cloning هستة مركزی تكنولوژی DNA نوتركیب را تشكیل میدهد كه با استفاده از آن میتوان یك ژن بیگانه را در یك سلول زنده كپی و تكثیر كرد و سپس با بیان آن، پروتئین مرتبط با آن ژن را كه اصطلاحاً، پروتئین نوتركیب (Recombinant Protein) نامیده میشود، در مقادیر زیاد تولید كرد.
کلون سازي DNA شامل جداسازي قطعه موردنظر از DNA و تکثير دادن نسخه هاي متعددي از آن در يک ارگانيسم (معمولا يک باکتري) است که طي دوره اي طولاني در آزمايشگاه قابليت رشد دارد. اين کار به منظور توليد مقادير نسبتا بالايي از قطعه مورد نظر DNA است که امکان تجزيه و تحليل ساختار و عملکرد آن را فراهم مي کند.
با استفاه از اين تکنيک، توالي خاصي از DNA به نام DNAنوترکيب توليد مي شود. در اوايل دهه ۱۹۷۰ تشخيص داده شد که ميکروب هاي معيني واجد آنزيم هايي به نام آنزيم هاي محدود کننده هستند که قادرند DNA را در يک ناحيه خاص برش دهند.اين بخش هاي بريده شده در فرآيندهاي بعدي براي ساختن مولکول هاي DNA نوترکيب مفيدند. اين خاصيت آنزيم هاي محدود کننده در فناوري DNA و کاربرد آن در ژنتيک پزشکي نقش دارد.
رابطه ی بین DNA و پروتئین
از روی DNA و اطلاعات موجود در آن ، پلی پپتید ( پروتئین )ساخته می شود. از آنجائیکه جایگاه DNA در هسته و محل پروتئین سازی در سیتوپلاسم قرار دارد و توسط غشاء هسته از یکدیگر جدا می گردد بنابراین مولکولی بایستی ارتباط این دو را برقرار سازد ، بر اساس دلایل زیر این مولکول ، RNA می باشد.
1-مولکول RNAکوچک بوده وبه راحتی از غشاء عبور می کند.
2-مقدار RNA در سلول هایی که فعالیت پروتئین سازی زیادی دارند ، بالا می باشد.
3- RNA هم در سیتوپلاسم و هم در هسته وجود دارد.
4- مقدار RNA در سلولهایی با پروتئین سازی کم ، اندک می باشد.
این مولکول میانجی که اطلاعات را از DNA به ریبوزوم حمل می کند، RNA پیک نام دارد.
فرآیند ساخته شدن RNA از روی DNA رونویسی نام دارد ، که اولین قدم برای ساخته شدن پروتئین می باشد. این عمل توسط آنزیم RNA پلیمراز صورت می پذیرد.
ساختار پروتئین ها
پروتئینها از اتصال اسیدهای آمینه به یکدیگر از طریق پیوند پپتیدی بدست میآیند. تشکیل پیوند پپتیدی و قرار گرفتن ترتیب اسیدهای آمینه که برای هر پروتئین اختصاصی است، به سادگی امکان پذیر نیست. به همین دلیل میبایست در یاخته مکانیسم ویژهای وجود داشته باشد که بتواند ویژگی پروتئینها را حفظ کند. بیوسنتز پروتئینها در واقع ترجمه ترتیب نوکلئوتیدی اسید نوکلئیک DNA در مولکول پروتئین است. انتقال اطلاعات از DNA به مولکول پروتئین بوسیله RNAها ، بویژه mRNA امکانپذیر است. بدین ترتیب برای هر پروتئین ، mRNA اختصاصی آن پروتئین وجود دارد. به عبارت دیگر هر پروتئین در روی DNA ، ژن اختصاصی دارد که اطلاعات آن ژن در mRNA رونویسی و در مولکول ترجمه میشود.
بیوسنتز پروتئین یا ترجمه Translation mRNA
فرآیندی است که طی آن اطلاعات موجود در mRNA برای ساخت پروتئین مورد استفاده قرار میگیرد.
عوامل لازم برای ترجمه
عوامل لازم برای ترجمه : 1- الگو( mRNA) 2- مصالح ساختمانی 3- آنزیمها 4- انرژی 5- فاکتورهای پروتئینی
فاکتورهای پروتئینی
به عوامل پروتئینی گفته میشود که در هریک از مراحل مختلف شروع، ادامه و خاتمة سنتز پروتئین شرکت میکنند. این فاکتورها برحسب مرحلهای که وارد آن میشوند به نام فاکتورهای شروع (IF) ادامه (EF) و خاتمه (RF) نامیده میشوند. تنوع فاکتورهای مختلف پروتئینی در یوکاریوتها بسیار بیشتر از پروکاریوتها است. به این ترتیب امکان تنظیم دقیق تر سنتز پروتئین در یوکاریوتها وجود دارد. به طور کلی مراحل سنتز پروتئین در یوکاریوتها و پروکاریوتها بسیار شبیه به یکدیگر و شامل مراحل زیر است: 1- مرحله شروع 2- مرحلة ادامه 3- مرحلة خاتمه
1- تشکیل کمپلکس آغازگر اولین واقعه برای سنتز پروتئین محسوب میشود.
2- برای انجام این مرحله به دو فاکتور طویل کننده نیاز است.
3- عمل طویل شدن خاتمه ادامه مییابد. فاکتورهای ختمRF) ) وارد عمل میشوند.
کاربرد تكنولوژی نوتركیب
1- درمان بیماری های ژنتیکی ( ژن درمانی)
2- تولید فراورده های بیولوژیکی مفید ( انسولین)
3- تولید واکسن
4- بهبود گياهان زراعي ، برخورد با گونه هاي ميکروبي نوترکيب...
سانتریفیوژ
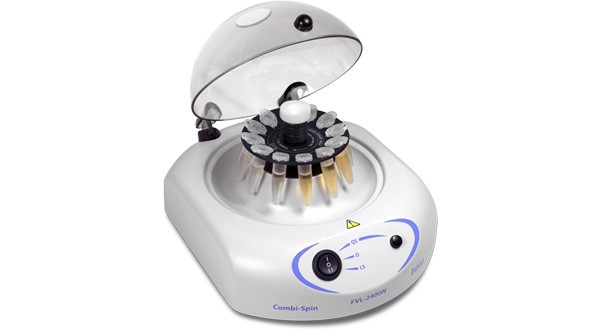
اولین باریک مهندس ارتش انگلیس به نام بنجامین روبینز ، دستگاه بازویی چرخشی برای شناسایی داروها ایجاد کرده بود . در سال 1879 ، انتونی پراندلنت، برای اولین بار سانتریفیوژهای امروزی را برای جداسازی خامه از شیر مورد استفاده قرار داد . در سال 1879 ، شخصی به نام گاستاف ، نشان داد که از سانتریفیوژ میتوان برای کارهای تجاری استفاده کرد . ابعاد مختلفی از سانتریفیوژ ها گسترش یافته است و طیف وسیعی از عملکردها را از میلی لیتر تا لیتر را می تواند مورد ارزیابی قرار دهد .
تصویرروبرواز یک سانتریفیوژ متعلق به قرن19 بوده که با دست می چرخید.
توجه به میکرو سانتریفیوژ ها ، در سال 1962 ، توسط یک شرکت آلمانی توسعه یافت و این شرکت سیستم میکرولیتری را برای اهداف ازمایشگاهی مورد استفاده قرار داد.
اصول سانتریفیوژ
چنانچه ذرات در يك نمونه داراي جرم هاي متفاوتي باشند، مي توان براساس اختلاف جرم و تأثير نيروي ثقل آنها را از يكديگر جدا کرد. براي تسريع اين عمل از روشي به نام سانتريفوژ يا ميان گريزش استفاده مي شود. مبناي اصلي سانتريفوژ، اصل گريز از مركز است كه يكي از اصول فيزيك دوران محسوب مي شود.
درحقيقت سانتريفوژ توسط نيروي گريز از مركز، ذرات سوسپانسيون را از مايع جدا مي كند. همچنين مي تواند باعث تفكيك دو مايع با تراكم متفاوت شود. اين مايعات مي توانند مايعات بدن باشند (مانند خون، سرم و ادرار).
سانتريفوژ با ايجاد نيرويي چندين برابر نيروي جاذبه، باعث افزايش سرعت طبيعي جدايي ذرات با تراكم متفاوت مي شود.
در یک نگاه، سانتريفوژ يك چرخنده فلزي است با حفره هايي كه در آن نمونه هاي مورد نظر قرار داده مي شود و داراي موتوري است كه با سرعت انتخاب شده مي چرخد.
سانتریفوژ چیست؟
سانتریفوژ یا دستگاه مرکزگریز دستگاهی است که در آن با استفاده از نیروی گریز از مرکز مواد را از یکدیگر جدا میکنند. در این دستگاه محفظهای که مواد جداشدنی در آن قراردارد معمولاً به کمک یک موتور به سرعت حول یک محور میچرخدواز آن برای چرخاندن مواد با سرعت بالا استفاده میشود. دانشمندان معمولاً دستگاه سانتریفوژ را برای جدا کردن ذرات جامد از یک مایع یا تقسیم مخلوط مایعات به اجزای مختلف آن به کار میگیرند.
مخلوط را درون لولهای قرار میدهند به طوری که با چرخش ، دستگاه به سمت خارج از مرکز حرکت میکند و به حالت افقی قرار میگیرد. در این حالت، نیروی گریز از مرکز میخواهد که مخلوط را برخلاف مرکز سانتریفوژ براند و از این نقطه دور کند.در این حال ذرات یا مایع سنگین تر بیش تر به سمت بیرون (یا ته مخلوط) رانده میشود. وقتی سانتریفوژ از حرکت باز میایستد، مواد به حالت غیر مخلوط باقی میمانند. خون و سایر نمونههای بیولوژیکی را معمولاً به وسیله دستگاه سانتریفوژ جدا میکنند
انواع دستگاههای مرکز گریز برای مصارف گوناگون ساخته شدهاست. نمونههای خانگی این دستگاه برای جداکردن آب از سبزیها مثل کاهو و غیره بکار میرود. در نمونههای آزمایشگاهی برای جداکردن گلوبولهای خون از پلاسما استفاده میشود. دستگاههای صنعتی با موتورهای قوی و در ابعاد بزرگ برای جدا کردن مواد بکار میرود. در کار غنیسازی اورانیوم نیز از دستگاههای مرکزگریز گازی استفاده میشود
تقسیم بندی سانتریفوژها برحسب سرعت چرخش
1 سانتریفوژهای با دور بالا
2 سانتریفوژهای با دور پایین
3 سانتریفوژهای اولترا
سانتریفوژهای با دور بالا
دور دوران آن بینrpm24000-21000و حداکثر rpm 30000است.سانتریفوژهای دور بالا برای بیشتر فرآورده ها استفاده می شود . همگی یخچال دار می باشند.
دو نوع سانتریفوژ با دور بالا وجود دارد: کم ظرفیت و پرظرفیت.
سانتریفوژ کم ظرفیت :با نمونه برداری گسسته می تواند میکروارگانیزم ها، سلول ها، ویروس ها و ارگان های سلولی را جدا کند.
سانتریفوژ پرظرفیت:مدل پیوسته ای است برای به دست آوردن مخمر و باکتری ازمحیط کشت، پروتئین از نمونه ها و ویروس و باکتریوفاژ از نمونه های رقیق شده. (2)
سانتریفوژهای با دور پایین
دور دوران آن بین rpm 2000-6000 با حداکثر rpm 8000 در هر دو فرم یخچال دار و بدون یخچال موجود هستند.بیشتر برای سانتریفوژ کردن سلول های خونی یا ذرات حجیم استفاده شده و برای جداسازی ذرات ریز سرعت آن کافی نیست.
سانتریفوژهای اولترا
در اولترا rpm 100000-75000 با حداکثر rpm 120000 است.برای تفکیک مواد تشکیل دهنده سلولی کاربرد دارند. همگی دارای یخچال است. زیرا در دورهای بالا اصطحکاک(1) هوا باعث گرم شدن دستگاه و درنتیجه تخریب پروتئین ها می شود. اولتراها معمولا در مراکز تحقیقاتی استفاده می شوند.
خواص سانتریفیوژها بر اساس چرخش انها:(جدول1)
|
خواص |
الترا سانتریفوژ |
دور بالا |
دور پایین |
|
سرعت(rpm*1000) |
120-75 |
30-21 |
8-2 |
|
یخچال |
همگی |
همگی |
برخی مدل ها |
|
سیستم خلا |
همگی |
برخی مدل ها |
خیر |
|
شتاب دهنده |
اغلب |
اغلب |
برخی |
در تقسیم بندی دیگر سانتریفوژ ها را به سه نوع شناور ،زاویه ثابت ومحوری تقسیم می کنند:
سانتریفوژهای شناور:
در این نوع سانتریفوژ، در حالت توقف وضعیت عمودی و در حالت دوران نمونه ها وضعیت افقی با سطح زمین دارند.
در این نوع سانتریفوژ، ذرات معلق بر اثر نیروی گریز از مرکز به بخش خارجی، یعنی انتهای لوله ها رانده می شوند و رسوب به صورت یک لایه تقریبا یکنواخت در ته لوله تشکیل می شود. در پایان عمل، لوله های حاوی نمونه مجددا به حالت عمودی درآمده، رسوب در ته لوله و محلول شفاف در بالای آن قرار می گیرد.
سانتریفوژهای زاویه ثابت:
در این نوع سانتریفوژ لوله حاوی نمونه نسبت به محور دوران یک زاویه ثابت دارد. این زاویه از 25 تا 45 درجه می تواند متغیر باشد و ذرات معلق براثر نیروی گریز از مرکز به سمت خارج محور دوران رانده می شوند اما برخلاف سانتریفوژهای شناور رسوب در جدار و بخشی از کف لوله که در قسمت خارجی محور دوران قرار دارد، رانده می شود.
البته هر قدر این زاویه نسبت به محور دوران کمتر باشد، رسوب بیشتر در جداره تشکیل می شود و اگر زاویه بیشتر باشد، رسوب بیشتر در کف تشکیل می شود.
شکل روتوردر این نوع سانتریفوژ اجازه دوران در دور بالاتر و رسوب ذرات ریزتر را می دهد. لذا میزان رسوب دهی این نوع سانتریفوژ از نوع شناور بالاتر است.
اگر در نوع شناور بخواهیم مانند زاویه ثابت، از دور بالاتر استفاده کنیم در اثر اصطکاک بیشتر با هوا، درجه حرارت افزایش خواهد یافت.
سانتریفوژهای محوری:
در اصل لوله حاوی نمونه در طول محور عمودی خود دوران می کند (برخلاف سانتریفوژهای معمولی که در طول محور افقی دوران می کنند).
کاربرد انواع مختلف سانتریفوژها:(جدول2)
|
جداسازی/نوع |
الترا سانتریفوژ |
دور بالا |
دور پایین |
|
سلول |
بله |
بله |
بله |
|
رسوب |
همگی |
اغلب |
برخی |
|
قطعات غشا |
همگی |
برخی |
خیر |
|
ریبوزوم-پلی زوم |
همگی |
برخی |
خیر |
|
ماکرو ملکول |
همگی |
برخی |
خیر |
اجزای دستگاه سانتریفیوژ:
1.موتور(پمپ) 2.روتور 3.یخچال 4.سیستم کنترل 5.محفظه دستگاه
روتور:
سانتریفوژ معمولی دارای محفظه ای بنام روتور یا سر است که با موتور کار می کند . روتور ها دارای انواع مختلفی هستند ولی انواعی که معمولا در آزمایشگاه ها مورد استفاده قرار می گیردبه دو دسته تقسیم می شود: دسته اول روتور هایی که در آنها لوله محتوی مایع محکم در یک زاویه ثابت نگاه داشته می شود و به همین جهت آنها را روتورهای با زاویه ثابت می گویند. دسته دوم آنهایی هستند که لوله هایشان در محفظه های فلزی قرار دارند و با چرخش روتور به خارج تاب خورده وبه صورت افقی قرار می گیرندو به این ترتیب مایع و مواد معلق درون این لوله ها در معرض نیروی گریز از مرکز واقع می شوند.این روتور ها را روتور با محفظه آویزان می گویند.
وقتی جسمی با شتاب می چرخد ،از لحاظ فنی ،نیروی مرکزگرا سبب حرکت جسم در مسیر دایره ای با شعاع ثابت می شود و این نیرو دائما جسم را به طرف مرکز دایره چرخش می کشاند.هنگامی که سرعت ثابت است، این نیرو فقط سبب تغییر جهت حرکت می شود.از طرفی جسم نیز با نیرویی به نام مرکز گریز در مقابل تغییر جهت حرکت به سمت خارج کشیده می شود که اندازه آن مساوی نیروی مرکزگرا است و موجب گرایش جسم به فرار از مسیر منحنی الخط دایره چرخش در راستای مستقیم و مماس بر دایره می شود
مشخصات روتور مناسب برای روش های مختلف سانتریفوژ در جدول3 ارائه شده است
|
نوع روتور |
ایزوپیکریک |
منطقه ای |
رسوب دهی تمایزی |
|
زاویه ثابت |
خوب |
ضعیف |
عالی |
|
عمودی |
خوب |
خوب |
ضعیف |
|
شناور |
کافی |
خوب |
ناکارآمد |
|
ناحیه ای |
کافی |
عالی |
ضعیف |
کاربرد سانتریفوژ
در شکر سازی شربت بسیار غلیظ ماسکوبیت از دو بخش جامد (بلورهای شکر) و مایع (بخش غیرکریستالی) تشکیل یافته است که در عمل سانتریفوژ این دو بخش از یکدیگر جدا می شوند. کریستالهای شکر شسته می شوند و در این صورت شکر با درجه خلوص بالا تولید می شود.
پس آب این بخش، بدلیل اینکه دارای مقادیر قابل توجهی شکر است طی چند مرحله مجددا کریستال گیری شده، در نهایت پس آبی که دیگر نمی توان از آن کریستال گرفت به عنوان ملاس از کارخانه خارج می شود. در برخی از کارخانجات این ملاس به واحد قندگیری از ملاس رفته و باکمک پودر آهک قند ملاس بازیافت می شود . در کارخانجاتی که تولید قند دارند، سانتریفوژهایی جهت تبدیل شکر به قند فعالیت دارند
سانتریفوژهادر تمام قسمت هایی که احتیاج به جداسازی باشد وجود دارند و مثال دیگر کاربرد آن در صنایع غذایی در کارخانه های فرآورده های لبنی است.
- در صنایع نشاسته سازی،رنگ رزی،بافندگی جهت خشک کردن مواد شیمیایی داروئی،لباس و غیره نیز کاربرد دارد.
· از سانتریفوژ می توان به عنوان کنترل کننده آلودگی هوا در محل تولید آن نیز بهره برد.
انواع سانتریفوژ های مورد استفاده که در منابع فاضلاب و لجن فعال کاربرد دارند
1-سانتریفوژهای جامد کاسه ای(استوانه ای)
2-سانتریفوژهای سبدی(سبدی سوراخ دار-سبدی بدون سوراخ)
3-سانتریفوژ دیسکی
سانتریفوژ استوانه ای
سانتریفوژ استوانه ای(کاسه لوله ای) یکی از انواع مهم است که در عین سادگی می تواند نیروی سانتریفوژ زیادی ایجاد کند .سانتریفوژهای استوانه ای را می توان سرد کرد که در کار کردن با پروتئین یک مزیت به حساب می اید .
در این نوع سوسپانسیون معمولا از انتهای لوله وارد می شود و مایع شفاف شده از بالای ان خارج می شود جامدات موجود در محلول به صورت یک لایه خمیر ضخیم بر روی دیواره لوله تشکیل می شوند تا زمانی که در خروجی جسم جامدی مشاهده نشود می توان به تزریق خوراک ادامه داد پس از این مرحله سانتریفوژ را خاموش کرده وتمیز می کنند. این وقفه در انجام عملیات یک ایراد مهم بحساب می اید
تحلیل کارایی سانتریفوژ
نیروی سانتریفوژ:
:نیروی گریز از مرکز
:جرم جسم
:شتاب گریز از مرکز
:فاصله جسم از محور چرخش
:سرعت چرخش (رادیان در واحد زمان)
سرعت ته نشینی ذرات در معرض نیروی گریز از مرکز
=سرعت ته نشینی
=قطر ذرات کروی
=چگالی مایع در حال چرخش
µ =چگالی مایع
=ویسکوزیته مایعات
سانتریفوژ استوانه ای
b=طول بخش استوانه ای
r= فاصله عمودی از محور چرخش
Rc= فاصله شعاعی از محور چرخش به لایه بالای کیک
RL=فاصله شعاعی از محور چرخش به سطح مایع
Rw= فاصله شعاعی از محور چرخش به دیوار سانتریفوژ
مدت زمان اقامت یک مایع در یک سانتریفوژ استوانه ای
V=حجم سانتریفوژ در دسترس مایع
Q=حجم میزان جریان مایع از طریق سانتریفوژ
معادله اصلی سانتریفوژ استوانه ای(دبی خوراک ورودی)
سرعت ته نشینی فقط تابعی از ذرات می باشد و مستقل از سانتریفوژ خاص مورد استفاده می باشد ولی مقدار موجود در کروشه که بد ان طول می باشد تابعی از ذرات نمی باشدو فقط به نوع سانتریفوژ وابسته است
فیلترسانتریفوژها و معادلات طراحی آنها
فيلتر سانتريفوژي (Centrifugal filter)
- اين فيلتر ها به دو نوع كلي پيوسته و ناپيوسته تقسيم مي شوند . به طور كلي معمولاً اين فيلتر ها در مورد جامداتي كه يك قالب متخلخل تشكيل مي دهند مورد استفاده قرار مي گيرد. براي اين كار دوغاب را وارد يك سبد چرخان مي كنند كه داراي يك ديواره شياردار يا مشبك است و يا محيط فيلتر با پارچه يا توري فلزي پوشانده شده است.
انواع فیلترسانتریفوژها
- فیلترسانتریفوژ ناپیوسته
- فیلترسانتریفوژ پیوسته
فیلترسانتریفوژ معلق از بالا(ناپیوسته)
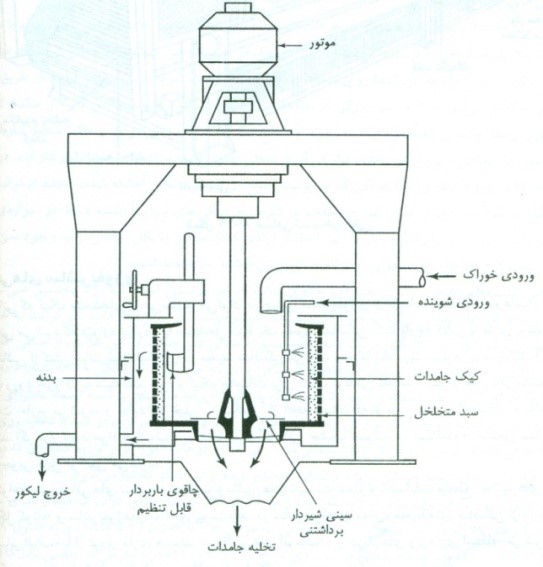
فیلترسانتریفوژ با نوارنقاله رفت و برگشتی(پیوسته)
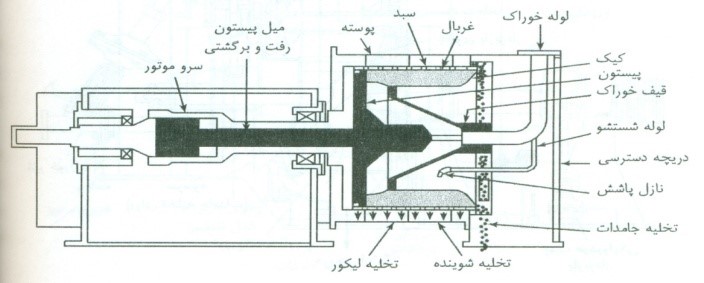
فیلتراسیون
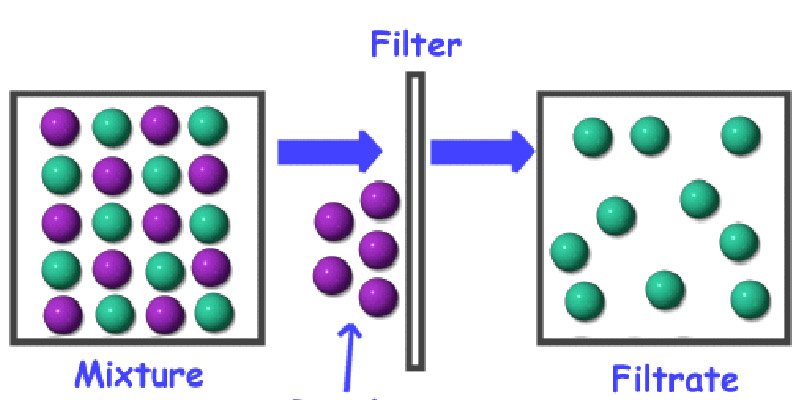
مقدمه
فیلتراسیون بعنوان یک روش مکانیکی برای جداسازی یک یا چند ترکیب از یک سیال بر اساس اختلاف اندازه ،آنها شناخته میشود.
با توسعه غشاهای مورد استفاده در این فرایند از این تکنیک برای جداسازی مواد محلول در یک حلال یا جداسازی مخلوط گازها از یکدیگر استفاده میشود.غشا به عنوان یک جداکننده دو فاز عبوری وغیر عبوری مطرح است و میتوانند بر اساس خصوصیات زیر طبقه بندی شوند:[3]
1)طبیعت غشا (طبیعی یا مصنوعی )
2)ساختار غشا (متخلخل یا غیرمتخلخل )
3)کاربرد غشا (جداسازی فازهای گازی ،مایع و جامد )
4)مکانیزم فعالیت غشا (جذبی ،نفوذی ،تبادل یونی )
مزایای فرآیند فیلتراسیون:
1-عدم ایجاد تغییر در فاز یا حالت نمونه در طی فرآیند.
2-مصرف پایین انرژی.
3-تامین انرژی موردنیاز تنها با استفاده از الکتریسیته.
4-عدم نیاز به تجهیزات تغییر فاز همچون بخارسازها،کندانسورها و...
5-امکان اجرا در دماهای پایین.
6-عدم تغییرات PH و قدرت یونی در طی فرآیند
طبقه بندی انواع فرآیندهای فیلتراسیون:
انواع فرایندهای فیلتراسیون بر اساس اندازه ذرات و یا مولکولهای جداشونده طبقه بندی میشوند که مهمترین روشهای جداسازی غشایی عبارتند از :
اسمز معکوس ،نانو فیلتراسیون ،اولترافیلتراسیون ، میکروفیلتراسیون ،دیالیز و الکترودیالیز
جدول نیرومحرکه فرآیندهای غشایی :
روش های فیلتراسیون :
1- روش عمودی
در این روش خوراک بطور عمودی بر سطح فیلتر وارد میشود و از فیلتر عبور میکند،ذرات در روی سطح فیلتر ته نشین میشوند،به مرور زمان و در طی انجام فرایند ضخامت کیک تشکیل شده روی سطح فیلتر افزایش میابد که در اکثر موارد کیک تشکیل شده از نوع تراکم پذیر بوده ورابطه خطی بین ضخامت کیک و افت فشار وجود ندارد در نتیجه به مرور زمان سرعت فرایند فیلتراسیون کاهش شدیدی میابد و تخلیه کیک امری ضروری است وباعث افزایش زمان انجام فرایند میشود.[2]
2-جریان مماسی
روش دوم تکنیک جریان مماسی که دران جریان خوراک موازی با سطح فیلتر است و دراین روش تشکیل کیک به حداقل میرسد.دراین روش خوراک وارد فیلتر شده و دو جریان خروجی یکی عبور کرده از صافی(محلول رقیق یا filtrate) دیگری جریان رسوبی(محلول غلیظ)وجود دارد وازتشکیل کیک در سطح فیلتراسیون جلوگیری میشود که باعث افزایش فلاکس جرمی می شود.
مقاومت کیک های تراکم ناپذیر:
اگر کیک تراکم ناپذیر باشد ،ضخامت کیک با حجم فیلتر شده مستقیما متناسب و باسطح فیلتر نسبت عکس خواهد داشت.
مقاومت کیک های تراکم پذیر :
تمامی کیکهایی که از مواد زیستی تشکیل میشوند تراکم پذیر بوده و با فشرده شدن این کیکها سرعت فیلتراسیون کاهش میابد.در کیک های تراکم پذیر مقاومت کیک به صورت تابعی از افت فشار است
انواع تجهیزات و سیستم ها:
سیستم های فیلتراسیون به دو دسته کلی سیستم های آزمایشگاهی و صنعتی تقسیم میشوند و در این فرایند از تجهیزات با 5 طرح مختلف استفاده میکنند که به صورت زیر تقسیم بندی میشوند:
1-سیستم های فیلتراسیون استوانه ای
2-سیستم های فیلتراسیون فیبر توخالی
3-واحدهای تخت
4-سیستم های مارپیچی
5-سامانه های خاص
تجهیزات آزمایشگاهی:
از این تجهیزات برای فیلتر کردن سریع نمونه هایی با حجم کم استفاده میشود،در آنها نیرو محرکه توسط نیروی گریز از مرکز سانتریفوژ تامین میشود.نمونه در قسمت بالای سل که شامل غشا نیز هست قرار داده شده و با استفاده از یک سانتریفوژ فرایند فیلتراسیون انجام میشود.
از این تجهیزات در آزمایشهای کلینیکی و آنالیتیکال برای نمونه های با حجم کم استفاده میشود،هیچ کنترلی بر پدیده پلاریزاسیون غلظتی نیست و این آزمایشات اطلاعاتی درباره فلاکس عبوری از فیلتر نمی دهد. [3]
تجهیزات با مقیاس بالاتر، دراین تجهیزات پدیده پلاریزاسیون غلظتی توسط یک همزن کنترل میشود.همزن مغناطیسی در نزدیکی سطح غشا قرار میگیرد وپیوسته محیط هم زده میشود.دراین تجهیزات به دلیل کنترل پدیده پلاریزاسیون غلظتی فلاکس عبوری بالا است.
تجهیزات صنعتی:
1-مدل تخت
2-سیستم های استوانه ای
3-فیلترهای فیبر توخالی
4-سیستم های مارپیچی
5-سیستم های خاص
مدل تخت :
از لحاظ ساختاری از ساده ترین هستند،به این سیستم ها صفحه مسطح یا قاب و صفحه گفته میشود.در این فیلترها دو طرف یک صفحه تخت صلب،دو لایه از غشا قرار گرفته که بین صفحه صلب و غشا با استفاده از یک ماده فضا دهنده پر شده و تعدادی از این صفحات در یک فضای بسته قرار داده شده.جریان دراین فیلترها آرام است.تعویض غشاها دراین نوع فیلترها معمولا آسان است.
از لحاظ دانسیته فشردگی،مصرف انرژی و هزینه حد واسط سیستمهای استوانه و مارپیچی هستند
فیلترهای استوانه ای:
این سیستم ها معمولا توسط شکل دهی پلیمرها در یک غالب پلاستیکی یا کاغذی تهیه میشوند.بیشتر از غشاهای سرامیکی استفاده میشود.خوراک از درون لوله ها جریان میابد ومایع صاف شده از دیواره فیلتر لوله ای خارج میشود.در این نوع از فیلترها چندین فیلتر را میتوان در یک نگهدارنده واحد قرار داد.قطر فیلتر و اندازه آن با توجه به حداقل مصرف انرژی و هزینه ساخت انتخاب میشود
فیلترهای فیبر توخالی:
غشاهای فیبری توخالی از لحاظ ظاهری شبیه غشاهای استوانه ای هستند اما یک اختلاف اساسی با هم دارند،این نوع غشاها بر خلاف غشاهای استوانه ای خودنگهدارنده هستند.در این فیلترها خوراک از درون فیلترهای تو خالی جریان یافته و مایع صاف شده در جهت شعاعی از دیواره فیلتر خارج میشود.
فیلتر معمولا شامل یک جریان ورودی،یک جریان خروجی مایع باقی مانده و دو مسیر برای مایع صاف شده است.جریان خوراک و مایع صاف شده میتواند همسو یا ناهمسو باشد.معمولا 3000-50 فیبر مجزا را میتوان در یک محفظه اصلی جا داد.در اغلب موارد جریان از نوع آرام است.افت فشار با توجه به شدت جریان و طول غشا20-5psi است.در بین تمامی مدلهای فیلتر،این نوع مقدار نسبت سطح به حجم بالایی دارند.نگهداشت حجمی در آن پایین است. از لحاظ مصرف انرژی بسیار پایین است.به علت باریک بودن مسیر جریان وبالا بودن سرعت جریان شدت تنش بالا است.[2]
سیستم های مارپیچی:
از فشرده ترین و ارزان ترین ،سیستم های فیلتراسیون هستند.بطور گسترده کاربرد دارند.در دو طرف یک صفحه تخت صلب دو غشا تخت قرار گرفته که از سه ضلع بسته شده است و از طرف لبه باز به یک هسته مرکزی متصل شده اند و غشا به دور هسته مرکزی پیچانده شده.مایع صاف شده بعد از عبور از غشا به هسته مرکزی وارد میشود.غشا پیچانده شده به دور هسته مرکزی در درون یک پوسته فلزی یا پلاستیکی که تحمل فشار بالا را دارد قرار گرفته.یک راه افزایش سطح فیلتر بدون نیاز به افزایش طول آن استفاده از چند غشا با یک هسته مرکزی مشترک است.جریان در این نوع فیلترها از نوع آشفته است[1]و[2]
سیستم های خاص :
سیستم هایی که در MF و UF مورد استفاده قرار میگیرند باید طوری طراحی شوند که پدیده پلاریزاسیون و پدیده آلودگی را به حداقل برسانند.یک روش کاهش پدیده پلاریزاسیون و افزایش شدت جریان ،حرکت غشا است که باعث بوجود آمدن طرحهای متفاوتی در فیلترها شده است:
1-سیستم های گردشی
2-سیستم های ارتعاشی
3-سیستم های Dean Vortices
سیستم های گردشی :
دراین مدل غشا درون یک سیلندر قراردارد وحول یک محورگردش میکند.خوراک از فضای بین دو سیلندر عبور کرده و مایع صاف شده از غشا عبور میکند.در یک سرعت گردشی مشخص پدیده ورتکس تیلور ایجاد میشود که به واسطه ان شدت تنش ایجاد شده 100000 است که تقریبا ده برار بیشتر از فیلتر های معمولی است.این تجهیزات برای مقیاس های نیمه صنعتی وکوچکتر در صنایع دارویی و بیوتکنولوژی مناسبند اما به دلیل مشکلات مکانیکی مربوط به سیلندرها و نسبت سطح به حجم پایین و دانسیته کم غشا ها قابل افزایش مقیاس به حجم صنعتی نیستند.
نوع دیگر سیستمهای گردشی فیلترهای صفحه مسطح چرخان است که برای کاربردهای صنعتی مناسبند.در این نوع فیلترها غشا در بین دو صفحه دیسک صلب گرداننده قرار دارد که در اثر گردش دیسکها تنشی بالغ بر 400000 ایجاد میشود و مایع صاف شده از درون غشا عبور میکند.
فیلترها ی ارتعاشی:
یک روش دیگر به حرکت درآوردن غشا استفاده از تکنیک V-SEP است.این مدل شامل یک سری غشاهای صفحه تخت است که توسط لایه ای به قطر 1-2mm از یکدیگر جدا شده اند.نمونه های صنعتی این نوع فیلترها تا 150دیسک باسطح 30مترمربع میتواند داشته باشد .شدت تنش در سطح غشا تا 150000 میرسد.این تنش زیاد برای تغلیظ زیاد نمونه های مورد استفاده قرار میگیرد.
فیلتراسیون متداول:
نوعی از فیلتراسیون که در آن تشکیل کیک مهم و زیاد است ،معمولا حاوی ذرات بزرگتر یا ریز جاندارها میباشد .
تجهیزات مورد نیاز برای فیلتراسیون متداول :
1-فیلترها "صفحه و قاب“فشاری
2-فیلتر افقی صفحه ای
3-فیلتر عمودی ورقه ای
4-فیلتر شمعی
5-فیلتر خلا دورانی
فیلتر عمودی ورقه ای :
فیلتر عمودی ورقه ای که در شکل نشان داده است سطح کمی نیاز دارد اما باید در فضایی قرار گیرد که فضای بالای ان خالی بوده تا بتوان ورقه های فیلتر و کیک را خارج نمود. این فیلتر به ازای حجم موجود سطح فیلتراسیون بالایی را در اختیار می گذارد.
فیلتر شمعی :
لوله هایی که بر روی یک فیلتر مخزنی سوار میشوند طوری عمل میکنند که کیک بر روی سطح خارجی آنها تشکیل شده ومایع فیلتر شده در داخل لوله ها به سمت بالا حرکت میکند. این لوله ها با استفاده از "شستشوی در خلاف جهت" تمییز میشوند.
فیلتر خلا دورانی :
فیلتر خلا دوار را که برای حجم های زیاد فیتراسیون در جداسازی های زیستی بکار برده می شود.در مقیاس بزرگ استفاده می شوند جایی که مواد جامد به سختی فیلتر میشوند.به همین دلیل به میزان زیاد در عملیات تجاری مورد استفاده قرار میگیرند.از آنجایی که این فیلترها به صورت خودکار عمل میکنند هزینه های کارگری پایینی نیز دارد.فیلتر شامل یک استوانه دوار است که از انتها نشان داده شده است.فشار در خارج از این استوانه اتمسفریک میباشد اما در داخل استوانه یک خلا نسبی است. قسمتی از استوانه به صورت غوطه ور در محلول قرار داده می شود و در طول فرایند با سرعتی کم دوران میکند.مایع به درون استوانه مکیده میشود و جامدات موجود در محلول بر روی سطح خارجی استوانه تشکیل یک کیک می دهند.هنگامی که این کیک به خارج از ظرف محلول دوران میکند شسته و خشک شده وسپس از استوانه جدا میشود.مرحله جداسازی کیک از استوانه با استفاده از یک تیغه انجام می شود [3]
میکروفیلتراسیون
میکروفیلتراسیون یکی از فرآیندهای مهم غشائی میباشد که اساس کار آن جداسازی فیزیکی میباشد که اندازه مواد جامد حل شده و کدورت ومیکروارگانیسم های حذف شده به وسیله سایز منافذ غشاء ها از 0.2تا 20 میکرون تعیین شده است. در این روش جداسازی باکتریها ، مواد معلق کلوئیدی و مواد پلیمری حذف میشوند و ذرات میکرو که کوچکتر از منافذ غشاء هستند عبور میکنند.
روش میکروفیلتراسیون در صنایع زیر کاربرد دارد:
- پیش تصفیه برای نانوفیلتراسیون و اسمز معکوس
- تصفیه بیولوژیکی آبهای آلوده
- جداسازی جامد – مایع برای صنعت غذا و دارو
- استریلیزاسیون در نوشیدنی ها و داروها
- شفاف کردن آب میوه ها
اولترافیلتراسیون
اولترافیلتراسیون تکنولوژی جداسازی توسط غشا است که بر مبنای غشاء نیمه تراوا جهت جداسازی به کار برده می شود.این تکنولوژی جهت حذف ذرات ریز و آلودگیهای میکروبی می باشد. اختلاف فشار، نیروی محرک جریان، جهت عبور ازمیان غشا می باشد.
مزیت ها
سرعت جریان بالاتر (flux) و مقاومت بهتر در برابر آلودگی
تراکم بالا و انعطاف پذیری خوب
تحمل خوب شرایط اسیدی و گرمایی
مقاومت بهتر در مقابل باکتری ها
نگهداری در شرایط خشک
مقاوم در برابر عوامل اکسیدکننده
موارد اصلی کاربرد
پیش تصفیه سیستم های RO
پالایش و حذف باکتری در صنایع آشامیدنی، شیر و آب معدنی
تصفیه فاضلاب شهری و صنعتی
پالایش روغن موجود در سیکل آب برگشتی
بازیافت و تصفیه آب تبرید و تصفیه بیشتر آب در صنایع گوناگون
عمومیت کاربرد در سایر زمینه ها نظیر شیمیایی، برق، مواد غذایی، نفت و نساجی
فیلتراسیون آب شهری، رودخانه و دریا
اولترافیلتـراسیون
اولترافیلتراسیون یک فرایند غشایی میباشد. چنین فرایندی وابسته به قابلیت تراوایی غشا که مرتبط با اندازهی عبوری از غشا است، میباشد. فرایندهای مشابه این نوع نامهای مختلفی به خود گرفتهاند: اولترافیلتراسیون، اسمز معکوس، میکروفیلتراسیون، هایپرفیلتراسیون و دیافیلتراسیون. تلاشهای اخیر تفاوت بین این فرایندها را بر مبنای مواد جداسازی شده توسط آنها بیان مینماید که در شکل 5 این تقسیمبندی نشان داده شده است. با توجه به شکل، اشتراکات زیادی در بازههای اندازه ذرات دیده میشود.
فرایندهای اولترافیلتراسیون و موارد مشابه سه مشخصهی ویژه دارند: این فرایندها از جران متقاطع با سرعت زیاد استفاده میکنند، توسط نوع غشا شناخته میشوند و در تجهیزات واقعی وابسته به هندسهی غشا میباشند. هر کدام از این مشخصهها ارزش تأمل و بررسی دارند.
جریان متقاطع
فرایند اولترافیلتراسیون همواره شامل جریان متقاطع با سرعت زیاد روی سطح غشا و عمود بر شار عبوری از غشا میباشد. در حین عمل اولترافیلتراسیون تشکیل کیک موجب کاهش شار عبوری میشود و جریان متقاطع باعث کاهش تشکیل کیک بر روی غشا میگردد. کم بودن کیک در فرایند اولترافیلتراسیون باعث تمایز آن با فرایند فیلتراسیون معمولی میشود. هنگامی که یک محلول درشت محلول درشت مولکول تحت عمل اولترافیلتراسیون قرار میگیرد، جریان متقاطع باعث کاهش تجمع درشت مولکولها در نزدیکی سطح غشا میگردد. این تجمع، «قطبی شدن غلظتی» نامیده میشود که باعث افزایش فشار اسمزی و در نتیجه کاهش جریان عبوری از غشا میگردد.
غشاها
اولترافیلتراسیون شدیداً وابسته به نوع غشا میباشد که این حالت متفاوت با فیلتراسیون مرسوم است که در آن گزینهی فیلتر معمولاً تأثیر کمتری در جریان عبوری از میان کیک دارد. در اولترافیلتراسیون با توجه به اینکه جریان متقاطع باعث کاهش تشکیل کیک یا قطبی شدن غلظتی میشود، غشا نقش مهمی را ایفا میکند. از طریق پخش کردن یک لایه نازک از محلول آلی در آب، شیشه یا یک پایهی خنثی ساخته میشود. غشا تخلخلی معادل 80/0 داشته و متوسط اندازهی تخلخلها در بازهی 1/0 تا 1 میکرومتر میباشد. با اینکه تخلخل موجود در سطح بزرگتر از 1 میکرومتر به نظر میرسد، ولی انقباض منفذ در طول ماتریس اسفنجی باعث کاهش اندازهی مؤثر منفذ تا m 5/0 میگردد. غشاهای اولیه از این نوع از جنس استرهای سلولز بوده ولی ساختارهای مشابهی از دیگر جنسهای پلیمری مثل نایلون، پلی وینیل کلراید و اکریلونیتریل ساخته شدهاند. این پلیمرها پایداری غشاها را در بازهی وسیعی از pH، دما و حلالهای آلی بهبود بخشیدهاند. چنین غشاهایی توسط بازه وزن مولکولی (MWCO) مشخص شده و برای نمونه با اندازههای 1000، 10000، 100000 و 000/1000 دالتون در دسترس میباشند. غشاهای 100000 دالتونی عموماً برای جداسازی سلول مورد استفاده قرار میگیرند.
از کشش گرم فیلمهایی غیرمتخلخل پلیمری مثل پلی پروپیلن ساخته میشوند. لایهی پلیمری جهت تشکیل منافذ کوچکتر تحت کشش و گسیختگی قرار گرفته و ساختمان نهایی در نهایت شکل گرفته و سخت میگردد. این غشاها تخلخلی حدود 35% و ضخامت برابر 003/0 سانتیمتر دارند. با توجه به آبگریز بودن، این غشاها بایستی قبل از اولترافیلتراسیون محلولهای آبی توسط مخلوط آب ـ الکل آمادهسازی شوند. همچنین این غشاها بهترین نوع غشا جهت استفاده در دستگاههای قلب ـ ریه میباشند، ولی برای اولترافیلتراسیون بسیار رایج نمیباشند.
کمترین تخلخل (حدود 3%) را داشته و منافذ بیشتر به صورت تک توزیعی میباشند. از آنجایی که این غشاها معمولاً ده برابر نازکتر هستند، تراوایی مشابه با دیگر نوع غشاها را دارند. این غشاها با قرار دادن فیلمهای غیرمتخلخل از میکا یا پلی کربنات در معرض اشعهی آلفا ساخته میشوند. بخشهای اشعه دیده بر روی فیلمها توسط اسید هیدروفلوریک تحت تأثیر قرار گرفته و منافذ ایجاد میگردد.
تجهیـزات
مشخصهی سوم اولترافیلتراسیون، هندسهی غشا در تجهیزات واقعی میباشد. این هندسه، جریان متقاطع و مواد غشا را با هم پیوند میدهد تا اولترافیلتراسیون را مؤثر سازد.
این مدل شامل لایههای متناوبی از غشا، لایهی متخلخل نگهدارنده و محلهای توزیع برای خوراک و مایع عبوری است. واحد میتواند سطح مقطع مربعی یا بیضی داشته باشد و میتواند به صورت غشاهایی با سطح تا 1500 متر مربع در بازار عرضه گردد. این غشاها میتوانند برای تمیز کردن و یا تعویض غشاهای معیوب، از سیستم جدا گردند. این غشاها کمترین مقدار سطح بر واحد حجم انواع معمول را داشته و در نتیجه شار بر واحد حجم کمتری در فرایند اولترافیلتراسیون ایجاد مینمایند.
پیشنهاد دیگر استفاده از طرحهای به شکل پوسته و لوله میباشد. این ساختار مشابه مبدل حرارتی پوسته و لوله که دارای تعدادی لوله با انتهای متصل به یک صفحهی مشترک است، میباشد. جریان خوراک وارد مجرای لولهها شده و مادهی نفوذی از دیوار گذر میکند و مایع باقیمانده از دیگر انتهای لوله خارج میگردد. روی این هندسه تبلیغات گستردهای شده است. به عقیدهی ما این مدل معایب دیگر هندسهها را به صورت ترکیبی دارد. تمیز کردن و سرویس این نوع سختتر از حالت نوع صفحه و قاب میباشد و مقدار سطح به واحد حجم کمتری دارد و در نتیجه شارهای کمتری نسبت به مدل پیچشی و الیاف توخالی را داراست.
نوع سوم طرح پیچشی میباشد این طرح شبیه یک پاکت بزرگ از جنس غشا به همراه لایهی حد فاصل برای عبور خوراک میباشد. خوراک در اطراف پاکت تحت فشار زیاد در طول غشا جریان داشته و در داخل پاکت جمع میگردد. این مرحله آسان بوده، اما آنچه آن را پیچیده میکند این است که پاکت مسطح نیست و دور کانال مرکزی خوراک پیچیده شده است.
مایع عبوری از غشا به سمت داخل پاکت در جهت لوله جریان داشته و سپس به سمت انتهای واحد حرکت میکند. در نتیجه، دستگاه مشابه رولت میباشد که لایههای تعبیه شده برای عبور خوراک، غشا و فواصل حرکت مایع عبوری از غشا، حول یک لولهی مرکزی پیچیده شده و یک واحد فشرده با سطح غشایی تا 2000 متر مربع را تشکیل دادهاند.
طرح پیچشی اولترافیلتراسیون مقدار سطح به واحد حجم بسیار بزرگتر نسبت به طرح صفحه و قابل و ساختارهای لولهای دارد. در نتیجه شدت فیلتراسیون بر واحد حجم بیشتری بدست میدهند. این غشاها بسیار سختتر تمیز شده و اگر قسمتی از غشا آسیب ببیند کل غشا باید دور انداخته شود. در نتیجه هنگامی که خوراک تا حد نسبی خالص میباشد، متمایل به استفاده از این نوع غشاها میباشیم. به عنوان مثال میتوان به تولید آب فوق خالص با فرایند اسمز معکوس اشاره کرد.
شکل نهایی اولترافیلتراسیون ، طرح الیاف توخالی میباشد. این شکل شبیه دستگاههای غشایی لولهای میباشد که البته از لحاظ مقیاس متفاوت است. این الیاف معمولاً دارای قطر cm01/0 بوده، در حالیکه قطر لولهها در حدود cm1 میباشند. طرحهای اولترافیلتراسیون الیاف توخالی در تضاد با فرمهای صفحه و قاب هستند که در ابتدا بحث گردید. چون این الیاف مقدار سطح به حجم بسیار بالایی تا 3000 به غشا داده و باعث بدست آمدن بیشترین مقدار شار به واحد حجم میگردند. این دستگاهها به راحتی گرفته شده و به سختی تمیز میگردند. هنگامی که برخی از این الیاف از کار میافتند، کل ساختار غشا باید دور انداخته شود و قابل استفاده نمیباشد.
هر ساختاری برای شرایط ویژهای استفاده میگردد، ولی این به وضوح قابل تشخیص نیست. ما همواره نمیتوانیم پیشنهاد قابل اطمینانی داشته باشیم. به خصوص برای دو طرح پیچشی و الیاف توخالی، وجود مرحلهی پیش فیلتراسیون قبل از مرحلهی اولترافیلتراسیون امری ضروری است.
تمامی این طرحهای غشایی نیازمند تجهیزات اضافی
میباشند. هر فرایند شامل یک مخزن، یک پمپ خوراک و یک مدول غشایی است. پمپ باعث عبور جریان از روی غشا با شدت حداقل 10 برابر بیشتر از شار معمول عبوری از غشا شده و مخلوط باقیمانده دوباره به سیستم بازگردانده میشود. در مجموع میتوان گفت که ترکیبی از جریان متقاطع، نوع غشا و هندسهی آن بیانگر فرایند اولترافیلتراسیون و مبنایی برای تحلیلی که بحث خواهد گردید، میباشد.
انواع فرایندهای میکروفیلترسیون و اولترافیلتراسیون
1- عملیات غیرمداوم
2- فرایند یک مرحله ای
3- عملیات غیرمداوم همراه با خوراک دهی
4- فرایند چند مرحله ای با جریان برگشتی
عملیات غیرمداوم :
در این روش از یک پمپ برای خوراک دهی به فیلتر و گردش آن استفاده میشود و فرایند تا تغلیظ نهایی ادامه می یابد.در این فرایند با یک مبدل حرارتی در قسمت گردش محلول باقی مانده می توان دما را کنترل کرد.این سیستم ساده ترین روش برای تغلیظ یک حجم مشخص از یک نمونه است.در این سیستم فلاکس در حد بالا می باشد.از معایب این سیستم میتوان به انعطاف پذیری کم آن اشاره کرد.
فرایند یک مرحله ای :
در این روش مایع باقی مانده برگشت داده نمی شود در اغلب روش های UF وMF دبی جریان صاف شده از باقی مانده کمتر است راندمان در این روش بسیار پایین است.و برای بهبود آن نیاز به فیلترهای با سطح بسیار بالا است.از این سیستم در تصفیه پساب،حذف ترکیبات سمی و ... استفاده می شود .زمان اقامت نمونه در این سیستم در کمترین حد قرار دارد
عملیات غیرمداوم همراه با خوراک دهی :
در این سیستم در حین فرایند فیلتراسیون خوراک بطور پیوسته وارد می شود وسطح مایع در مخزن اصلی ثابت است از این سیستم در فرایندهای صنعتی استفاده میشود
زمان انجام فرایند غیرمداوم همراه با خوراک دهی بدلیل پایین بودن فلاکس نسبت به غیرمداوم بیشتر است در نتیجه نمونه باقی مانده به مراتب بیشتر پمپ می شود .
فرایندهای چند مرحله ای :
در این سیستم تنها غلظت در مرحله آخر بالا است و در مراحل قبل غلظت پایین و با حداکثر فلاکس کار میکند.افزایش بیشتر مراحل باعث بالا رفتن هزینه کنترل ، شیرها و لوله کشی میشود.زمان اقامت و حجم تانک مورد نیاز کمتر از سیستم ناپیوسته است. در این سیستم ها بطور متوسط در هر 24 ساعت کارکرد ، 1 تا 3 ساعت صرف .فرایند تمیز کاری میشود.
تخریب بیولوژیک میکروارگانیسم
- لیز آنزیم سلول ها
- تخریب سلولی توسط معرف های بیولوژیک
لیز آنزیم سلول ها:
مزیت های لیز آنزیمی سلول ها شامل :
گزینشی بودن
افزایش سرعت و بازده رهایش سلول
حداقل رساندن آسیب دیدگی محصول
شرایط pH و دمای ملایم تر
عدم تولید خرده های سلولی
برای لیز آنزیمی لازم است جزئیات ساختار فیزیکی و شیمیایی دیواره سلولی به خوبی مشخص شود.
هیچ آنزیمی توانایی تخریب کامل دیواره سلولی را ندارد.توانایی تخریب دیواره سلولی در باکتری های گرم مثبت و گرم منفی با یک دیگر متفاوت است.
بیشتر سیستم های لیز آنزیمی سلول ها در مقابل سلول های پیش تیمار شده یا در مقابل دیواره سلول ها فعال هستند.
محدودیت های اصلی سیستم های چند آنزیمی دسترس پذیری و هزینه بالای آنهاست.[13]
برای استخراج یک محصول معین از یک ارگانیسم ٬ انتخاب سیستم مناسب لیز سلولی به طبیعت دیواره لیز شده و طبیعت و جایگاه محصول در داخل سلول بستگی دارد.
ترکیب یک سیستم چند آنزیمی بازدهی و انتخابی بودن فرایند لیز سلولی را تعیین می کند.
در بخشی از فاز تولید ترکیب سیستم های لیز آنزیمی می توانند با القا گر های مختلف دست کاری شوند.
لازم است برای بهینه سازی فرایند لیز آنزیمی ،اطلاعات کمی مربوط به اثرات pH ٬دما ،غلطت آنزیم های لیتیک و سلول ها روی سرعت لیز سلولی بدست آورده شود.
هر چند مثل همه روش های غیر مکانیکی تخریب سلولی ٬ فرایند لیز آنزیمی خیلی کند است٬ولی نسبت به دیگر فرایندها ، سرعت و بازده استخراج محصول می تواند افزایش داده شود.
- اتولیز فرایندی است که سلول ها از قابلیت لیتیک خودشان استفاده کرده و آنزیم های لیتیک را تولید می کنند.
اتولیز مثل فرایند های خود هضمی خیلی کند است.
این فرایند با خشک کردن یا یخ و گرم شدگی سلول تسریع میشود.
اتولیز می تواند بوسیله پلاسمولیز ارگانیسم ها با سورفکتانتها٬ معرف های تیول و حلال های آلی مثل تولوئن و بوتانل یا دما تسریع شود.
پتانسیل اتولیز سلول ها متفاوت است ، اغلب آنها فاقد اطلاعات ژنتیکی تولید آنزیم های لیتیک هستند و بایستی از محیط خارج واز طریق روش های ژنتیکی ٬ ژن های کد کننده این آنزیم در داخل سلول وارد شوند.
سیستم های لیز سلولی که می توانند کلون شوند نه تنها شامل اتولیزن ها بلکه شامل آنزیم های کلیسین و فاژها نیز هستند. [13]
تخریب سلولی توسط معرف های بیولوژیک :
- با افزودن آنتی بیوتیک ها
- وارد کردن یک فاژ عفونت زا به سلول میزبان
- ممکن است سنتز دیواره سلولی با باز داشتن آنزیم های لازم یا آنتی بیوتیک هایی مثل پنی سیلین متوقف شوند. چنین معرف هایی ممکن است در انتها فاز رشد اضافه شوند تا با جلوگیری از سنتز دیواره و تکثیر سلول باعث لیز شدن آن شوند.
- آنتی بیوتیک های خاص سلول های باکتریایی را نفوذ پذیر می کنند ولی باعث لیز آنها نمی شوند. به عنوان مثال :
آنتی بیوتیک پلی ین و آنتی بیوتیک های پلی پپتیدی مثل پلی میاکسین ٬ گرامیسیدین ٬ تیروسیدین
- هیدرولیز دیواره سلولی میزبان با یک فاژ عفونت زا یک پدیده شناخته شده است.
تحت عفونت های شدید ممکن است تخریب سلولی قبل از وارد شدن اسید نوکلئیک فاژ به سلول اتفاق افتد. به هر حال به دلیل خطر احتمالی عدم کنترل عفونت، ورود فاژ به یک مقیاس صنعتی کاملا غیر منطقی و غیر قابل قبول است.
ترکیب فرایند های مختلف تخریب :
- به دو صورت مکانیکی و شیمیایی انجام میگیرد.
تیمارهای شیمیایی مثل تغییرات شدید pH و یا تیمار با شوینده ها:
نفوذ پذیری سلول را افزایش داده و باعث رهایش جزئی پروتئین ها می شود.
این فرایند ممکن است برای بازیافت محصولات محلول خاص کافی باشد ولی ممکن است برای رها سازی محصولات بیولوژیکی دیگر لازم باشد تخریب کامل سلولی انجام گیرد.
برای بازیافت محصولات گرانولاری مثل توده های متراکم باکتریایی، ذرات شبه ویروس مخمر و پلی هیدروکسی بوتیرات تخریب کامل سلولی لازم است.
- برای تخریب مکانیکی این محصولات به انرژی مکانیکی زیادی نیاز است و همچنین مراحل بعدی جداسازی را با مشکل مواجه می کند از این جهت از یک پیش تیمار شیمیایی مثل pH قلیایی ٬ افزایش غلظت کاتیون های یک ظرفیتی یا تیمار با شوینده ها استفاده می شود.
- با ترکیب روش های شیمیایی و مکانیکی تخریب موثر سلولها در فشار عملیاتی پایین و تعداد دفعات کمتر فراهم میشود.
روش های مکانیکی عموما برای تخریب دیواره سخت سلولی مناسب هستند.
اثرات شرایط بالا دستی روی تخریب ارگانیسم های مختلف :
- اثرات شرایط بالا دستی شامل اثر نوع میکرو ارگانیسم و شرایط محیط کشت آن روی تخریب است.
تخریب سلول های رشد داده شده در محیط کشت ساده راحتر از نمونه های رشد یافته در کشت های پیچیده صورت میگیرد.
مقاومت میکروارگانیسم ها نسبت به عمل تخریب به فاز رشد آنها و اندازه سلول بستگی دارد .
اثرات تخریب سلولی روی عملیات پایین دستی :
- یکی از مشکل ترین مسائل جداسازی جامد مایع ، حذف خرده های دیواره سلولی٬ غشاء سلولی و رسوب های پروتئینی٬ است.
تخریب و تیمار آنزیمی باعث کاهش خواص رسوب دهی سلول ها و خرده های سلولی ( 0.01 μm >) شده و باعث میشود که سانتریفوژ یا فیلتراسیون به علت تغییرات خواص سطحی٬ تراکم پذیری بالای جامدات٬ ویسکوزیته بالای سوسپانسیون و اختلاف دانسیته کم جامدات و سوسپانسیون کار آمد و موثر نباشد.
- برای افزایش بازده عمل سانتریفوژ وقتی که ذرات کوچکتر از 5 μm هستند باید :
1- سرعت جریان را کم
2- انعقادسازی اولیه انجام گیرد.
عمل فیلتراسیون ممکن است به صورت دورانی تحت خلاء و یا میکرو فیلتراسیون جریان متقاطع انجام گیرد.
استخراج دو فازی آبی برای بازیافت سلول های کامل یا خرده های سلولی از محلول های پروتئینی جالب است ولی هزینه بالا و بازیافت معرف ها در آن مشکل است.
شناخته شده ترین اجزاء فازی پلیمرهای محلول در آب و الکترولیت ها ، پلی اتیلن گلیکول٬ دکستران و پلی اتیلن گلیکول – فسفات است.
- تکنیک های جداسازی تحت تاثیر عوامل متعددی قرار می گیرد ولی اندازه متوسط ذرات و توزیع اندازه ذرات از مهمترین عوامل هستند.بیشترین مقدار رهایش پروتئین با افزایش میکرونی شدن خرده های سلولی افزایش می یابد.
- اندازه خرده های سلولی اثر مهمی روی فرایند های پایین دستی دارند.
- سوسپانسیون سلولی باید تحت شرایطی تخریب شود که از تخریب نا خواسته محصولات حساس آزاد شده از سلول ها تخریبی جلوگیری کند.از این رو لازم است بازدارنده های پروتئازی به سوسپانسیون اضافه شوند. تمام مواد شیمیایی که در همه مراحل تخریب و جداسازی به سوسپانسیون سلولی اضافه میشوند ممکن است روی محصول و عملیات بعدی اثر بگذارند.
- با پیشرفت اخیری که در زمینه تکنولوژی DNA نو ترکیب صورت گرفته٬ این امکان فراهم شده که تعداد زیادی پروتئین نو ترکیب درمانی به صورت توده های متراکم در سیتوپلاسم ٬ خصوصا اشریشیاکلی٬ تولید شده ودر داخل سلول تجمع یابد.
این توده های متراکم شامل پروتئین ها یا پلی پپتید ها یی است که به صورت دناتوره یا غیر فعال تجمع یافته اند.برای حل کردن آنها در محیط آبی از معرف های کائوتروپیک یا دترجنت ها استفاده میشود.
روش استاندارد جداسازی یک پروتئین بیان شده به صورت توده های متراکم با جداسازی این توده ها شروع میشود. بهترین تکنیک تخریب سلولی در این وضعیت هموژنایزر فشار بالا است.
- توده های متراکم معمولا با روش سانتریفوژ از اجزاء محلول و خرده های لیز سلولی جدا میشود.
- توده های متراکم پس از جداسازی با شوینده های رقیق یا معرف های کائوتروپیک مثل گوانیدین هیدروکلراید یا اوره شسته می شوند و غالبا معرف های احیا کننده (مثل دی یتوتریتول یا β- مکاپتواتانل) نیز برای تخریب پیوندها ی دی سولفیدی نادرست استفاده می شوند. سپس پروتئین محلول شده و احیا شده برای تخلیص و فعال سازی بعدی آماده است. [13]
مشخصات جداسازیهای زیستی

یک مشخصهی عمده و بارز زیست فناوری تنوع بسیار زیاد محصولات تولید شده میباشد. به عنوان مثال، یک شرکت پتروشیمی در حدود 10 گونه محصول تولید میکند، در حالیکه یک شرکت تولیدی دارویی بیش از 200 نوع محصول تولید میکند. ممکن است که تمامی این 200 محصول به صورت کاملاً زیستی تولید شده باشند؛ اما در بسیاری از موارد از تبدیلات زیستی تنها به صورت جزیی استفاده شده است.
تنوع این محصولات در جدول 1 آورده شده است. هرچند که این فهرست 10 سال قدمت دارد، با این وجود از بسیاری از شرکتهای زیست فنآوری موجود، قدیمیتر میباشد. اگر یک فهرست تازهتر و بهروز تهیه گردد، محصولاتی نظیر انسولین (که از لحاظ ژنتیکی اصلاح شده است)، هورمونهای رشد گاوی و انسانی و همچنین انترفرونها نیز به این فهرست افزوده خواهد شد و محتویات این فهرست نیز روز به روز اضافه میگردد.
جدول (1) انواع مولکولهای تولید شده توسط تخمیر
|
نوع مولکول |
تعداد گونهها |
|
آنتیبیوتیکها |
85 |
|
آمینواسیدها |
18 |
|
آنزیمها |
15 |
|
اسیدهای آلی و حلالها |
11 |
|
ویتامینها، مخمرها، فاکتورهای رشد و نوکلئوتیدها |
6 |
|
متفرقه ـ دکسترانها، بیواکسیدانهای استروئیدی |
8 |
|
|
143 |
این تنوع محصولات باعث گستردگی طیف وسیعی از روشهای جداسازی مورد استفاده میشود. مقایسهی فرایندهای جداسازی مورد استفاده در صنعت تخمیر به همراه طبقهبندیهای جامع و کامل در جدول 2 آورده شده است. این جدول نشان میدهد که 80% از روشهای جداسازی در فنآوریهای زیستی قابل استفاده میباشند. تمامی روشهای عملیاتی مرسوم شامل حالتهای پایدار و ناپایدار، تجهیزات پیوسته و ناپیوسته و جریانهای همسو و غیرهمسو نیز میتوانند مورد استفاده قرار گیرند. مقیاس این فرایندهای جداسازی، به شکل وسیعی گسترده میباشد. در مراحل اولیه، هدف اصلی نشان دادن و اثبات کارایی فرایند پیشنهاد شده میباشد تا بتوان اطلاعات مربوط به فرایند را کسب کرد و همچنین مقادیر کمی نیز جهت ارزیابی بازار و مطالعات کلینیکی تولید کرد. این کار در فازهای آزمایشگاهی و نیمه صنعتی انجام میشود. در مرحلهی بعدی، هدف اصلی تولید در مقیاسهای بزرگ و صنعتی و معرفی فرایند به صنعت جهت
تولیدات.تجاری.میباشد.
این فعالیتها در چارچوب مطالعات نیمه صنعتی و اقتصادی انجام میپذیرد.
جدول (2) طیف جداسازیهای مورد استفاده در بیوتکنولوژی
|
دستهبندی |
مورد استفاده برای تمامی مواد شیمیایی متداول |
مورد استفاده در جداسازیهای زیستی |
|
جداسازی فیزیکی |
7 |
7 |
|
جداسازیهای کنترلشونده از طریق تعادل |
22 |
18 |
|
جداسازیهای کنترلشونده توسط شدت |
13 |
10 |
|
|
42 |
35 |
در مواجهه با چنین تنوع و گستردگی، چگونه میتوان امیدوار به موفقیت بود؟
از طریق شناسایی دو خصوصیت مهم این فرایندهای جداسازی که در اکثر آنها نیز مشترک است. میتوان به جلو پیش رفت و امیدوار به کسب موفقیت بود. اول اینکه معمولاً ما با یک سوسپانسیون رقیق شروع میکنیم و سعی میکنیم که یک محصول خشک با خلوص زیاد تولید کنیم. جامدات موجود در این سوسپانسیون ممکن است حاوی ریز جانداران صدمه ندیده، قارچها و باکتریهای تکه شده، سایر ذرات جامد نامحلول و سوبسترای باقیمانده باشند. مایع سوسپانسیون نیز میتواند شامل پروتئینهای حل شده از محیط کشت باقیمانده، مواد واسط مسیرهای متابولیک و سایر محصولات مطلوب باشد. در بیشتر موارد محصول نهایی مورد نظر ما بلورهای بدون رنگ و بسیار پایدار میباشند.
دوم، تغییرات بسیار زیادی که بر روی خوراکهای رقیق در جهت تولید محصولات خالص انجام
میشود، نشان میدهد که این جداسازیها بسیار پیچیده و گرانقیمت میباشند. عملیات بازیابی و خالصسازی ممکن است بیش از سایر قسمتهای فرایند نیازمند تجهیزات پیچیده و نیروی انسانی باشد. واحد بازیابی معمولاً نیازمند سرمایهگذاری زیادی است و به همین دلیل، هزینههای جداسازی قسمت قابل توجهی از قیمت نهایی محصول را شامل میشود. بنابراین، فرایندهای بازیابی و خالصسازی باید به خوبی مطالعه و طراحی شوند.
با پاسخ دادن به سؤالات زیر طراحیهایمان را میتوانیم بهبود دهیم:
- ارزش محصول چیست؟
- کیفیت قابل قبول محصول چیست؟
- در هر جریان فرایندی، محصول کجا قرار دارد؟
- در هر جریان فرایندی، ناخالصیهای موجود کجا قرار دارند؟
- خواص نامتداول فیزیکی ـ شیمیایی محصولات و ناخالصیهای عمده کدامند؟
- از نظر اقتصادی، جداسازیهای جایگزین مختلف چگونه هستند؟
با در نظر گرفتن دقیق پرسشهای فوق، نکاتی حاصل میشوند که منجر به فرایندهای بهینه برای بازیابی محصول با کیفیت مناسب خواهند شد که در عین حال، با حداقل تلاش به میزان بالایی از بازیابی دست خواهیم یافت.
یک فراینـد ایدهآل
تنوع و گستردگی محصولات و جداسازیهای موجود در فنآوریهای زیستی سبب میشود که نتوان به یک شباهت کلی مابین بسیاری از فرایندهای مورد استفاده دست یافت و در بسیاری از موارد استثناهای زیادی نیز وجود دارد. با این وجود، این شباهتها یک روش برای فکر کردن در اختیار ما قرار میدهد، همانگونه که «جدول تناوبی» یک رابطهی را بین عناصر برقرار میکند.
با توجه به تجربههای حاصل شده میتوان گفت که اغلب جداسازیهای زیستی دارای چهار مرحلهی شبیه به یکدیگر میباشند که در پی یکدیگر رخ میدهند:
- جداسازی مواد نامحلول: فیلتراسیون و سانتریفوژ فرایندهای جداسازی اصلی مورد استفاده در این قسمت میباشند. در این مرحله، محصولات با غلظت نسبتاً کم و کیفیت پایین حاصل میشوند.
- جداسازی محصول: در این مرحله، مواد مختلف که خواصی متفاوت با محصول مطلوب دارند، جدا میشوند. افزایش قابل توجهی در غلظت و کیفیت محصول معمولاً اتفاق میافتد. جذب سطحی و استخراج با حلال نمونههایی از این دست فرایندها میباشند.
- خالصسازی اولیه: این روشهای جداسازی به صورت بسیار گزینشی نسبت به محصولات عمل کرده و ناخالصیهای با خواص فیزیکی و شیمیایی مشابه در مقایسه با محصول را از آن جدا میکنند. به عنوان مثال میتوان از کروماتوگرافی، الکتروفورز و رسوبگیری به عنوان موارد خوبی نام برد.
- خالصسازی نهایی: استفادهی نهایی محصول معمولاً تعیینکنندهی آخرین مرحله میباشد. در این مرحله معمولاً تبلور میتواند مورد استفاده قرار گیرد. همچنین اغلب محصولات نیز باید خشک شوند.
پایهی اصلی و ساختار این کتاب بر مبنای این چهار مرحله طراحی شده است:
یکی از راههای ارزیابی این چهار مرحله در نظر گرفتن غلظت و کیفیت محصولات تولید شده است. برای نمونه نمایی از فرآورش یک محصول خالص در جدول 3 آورده شده است. دقت شود که بیشترین افزایش در غلظت به مرحلهی جداسازی محصول مربوط میشود؛ اما کیفیت محصولات به شدت در مرحلهی خالصسازی اولیه افزایش مییابد. در برخی فرایندهای اخیر، این توالی متداول سادهتر شده و دو مرحلهی اول به صورت یک تک مرحله در نظر گرفته میشود. به عنوان مثال استخراج از محلول خروجی از تخمیر و تبادل یونی بستر سیال، به ترتیب در فصول 5 و 6 توضیح داده شده است.
جدول (3) نمایی از فرآورش و خصوصیات آنتیبیوتیکها*
|
مرحله |
محصـول |
||
|
نوع فرایند |
غلظت (g/lit) |
کیفیت (%) |
|
|
واکنش زیستی |
تخمیر |
5-1/0 |
0/1- 1/0 |
|
جداسازی مواد نامحلول |
فیلتراسیون |
5- 0/1 |
0/2- 2/0 |
|
جداسازی محصول |
استخراج |
50- 5 |
10- 1 |
|
خالص سازی اولیه |
کروماتوگرافی |
200-50 |
80- 50 |
|
خالص سازی نهایی |
تبلور |
200-50 |
100- 90 |
* غلظتها و کیفیتهای نشان داده شده به صورت نسبی بیان شدهاند. کیفیت ممکن است بیانگر خلوص محصولات فعالیت و یا درجهی تأثیر باشد.
طرحهایی که برای محصولات خارج سلولی بکار میروند، برای بازیابی مواد داخل سلولی باید اصلاح شوند. این عمل با بکارگیری یک مرحله جهت آزادسازی محصولات مطلوب از ریزجاندارها تکمیل میگردد. این آزادسازی معمولاً پس از جداسازی اولیه مواد نامحلول انجام میشود که باعث کاهش حجم میگردد. از آنجایی که پس از این آزادسازی، هنوز مخلوطی ناهمگون از مواد محلول و نامحلول وجود دارد، یک مرحلهی اضافیِ جداسازی ذرات جامد برای حذف کردن لاشهی سلول که نامحلول نیز میباشد، لازم و ضروری است. خروجی مایع که حاوی مواد مطلوب میباشد، به عنوان خوراک مرحلهی جداسازی محصول بکاررفته و مابقی مراحل فرایند تغییر نمیکند.
جداسازی باکتریهای عامل خوردگی بیولوژیکی
معمولاً شنیدن واژه میکروب و میکروارگانیسم، عوامل مسبب بیماریهای عفونی را به ذهن متبادر می کند ، امامیکروارگانیسمهای بیماریزا تنها حدود 0,1 درصد از کل میکروارگانیسمهای موجود در کره زمین را که بسیاری از آنها مفید بوده و حیات در کره زمین بدون آنها امکانپذیر نمی باشد ، تشکیل می دهند .
میکروارگانیسمها شامل باکتریها، مخمرها،قارچهای میکروسکوپی و ویروس ها هستند.
از این میان برخی باکتریها، مخمرها و قارچها(کپکها) مشکلاتی
برای سیستمهای صنعتی ایجاد می کنند که خوردگی میکروبی و
آلودگی سوخت و روانکارها از مهمترین آنها می باشد .
بیش از یک قرن است که نقش میکروارگانیسم ها در خوردگی فلزات مورد توجه محققین قرار گرفته است؛ اما علی رغم این زمان طولانی، هنوز نیز نقش آنها به درستی شناخته نشده است .
خوردگی میکروبیولوژیک در صنایع نفت از اولین مواردی است که توجه محققان را به خود جلب کرده است و تا مدتها ، تنها مورد عملی تحقیق رویMIC یا خوردگی تحت اثر میکروارگانیسمهاMicrobially) Influenced Corrosion) )
محسوب میشده است
خوردگی زیستی خوردگی میکروبی و یا خوردگی تاثیر پذیر از عوامل میکروبیولوژیکMIC=Microbiologically influenced corrosion
می تواند به عنوان فرایندی الکتروشیمیایی تعریف شود که در آن میکروارگانیسمها قادر به شروع، تسهیل یا تسریع واکنش خوردگی بدون تغییر در طبیعت الکتروشیمیایی آن می باشند.
محققان اعلام کرد ه اند که حدود20 تا 40 درصد از خسارات خوردگی، ناشی از خوردگی میکروبیولوژیک است. بنابراین می توان این جنبه از خوردگی را مخرب ترین نوع خوردگی دانست.
. این مسئله علتهای مختلفی دارد که مهمترین آنها عبارتند:
-1 وجود میکروارگانیسمها در تمام محیطها
-2 عدم شناخت دقیق اثر میکروارگانیسمها
-3 حساسیت اکثر آلیاژها و فلزات صنعتی
میکروارگانیسم ها قادرند بطور فعال محیط اطراف سطح فلز را تغییر داده تا فرایند خوردگی را تسهیل کنند . دخالت میکروبها در خوردگی به ندرت از طریق یک مکانیسم تنها و یا تنها توسط یک گونه از میکروارگانیسم ها انجام می شود . این میکروارگانیسمها می توانند در اکثر سیستمها با تبدیل و تغییر شرایط محیطی موجب بروز یا تشدید خوردگی شوند؛ بطور
مثال اثر خورنده میکروارگانیسمها در سیالات هیدرولیکی ، قسمتمهای مختلف موتورکشتی ها و دیگر سیستمهای استراتژیک کاملا به اثبات رسیده است . عوامل بیولوژیکی که موجب خوردگی در محیطهای مختلف میشوند به طور خلاصه با ذکر یک یا چند نمونه از آنها در جدول زیر ذکر شده اند.
|
Desulfovibrio |
1-باکتریهای احیا کننده سولفات |
الف) باکتریهای بیهوازی |
میکرو- ارگانیسمهای پروکاریوتیک |
|
Dethiosulfovibrio |
-2 باکتریهای احیا کننده تیوسولفات |
||
|
Thiobacillus |
-1 باکتریهای اکسید کننده گوگرد |
ب ) باکتریهای هوازی |
|
|
Gallionella |
-2 باکتریهای اکسید کننده آهن |
||
|
Pseudomonas,Aeromonas, Shewanella putrefaciens |
-3 سایر باکتریها |
||
|
Hormoconis resinae Aspergillus |
الف)قارچها |
میکرو- ارگانیسمهای یوکاریوتیک |
|
|
Chlorella, Spirogyra |
ب) جلبکها |
||
|
Seaweeds, Hydroids,Bivalve molluscs, crustacea |
ارگانیسمهای چند سلولی یوکاریوتیک |
||
خسارات خوردگی برآورد شده در کشورهای پیشرفته صنعتی حدود 2 تا 4 درصد تولید ناخالصی ملی (GNP) آنها می باشد ولی برای کشورهایی نظیر ایران که معمولا از روشهای پیشگیرانه خوردگی استفاده نمی کنند، در بسیاری از موارد خسارتها و هزینه های ناشی از خوردگی در قالب خرجهای تعمیراتی نهفته است و میزان خسارات خوردگی می تواند تا 5 درصد تولید ناخالص ملی افزایش یابد که بر این اساس خسارت مستقیم خوردگی ایران در سال 1379 معادل 27500 میلیارد ریال بوده است.
برخی از روشهای عملی میکروارگانیسمها در آغاز کردن یا تشویق خوردگی عبارتست از:
1- تولید متابولیتهای اسیدی
2- تولید متابولیتهایی که قادرند ویژگیهای محافظتی لایه غیر آلی را کاهش داده یا بی اثر کنند
-3 افزایش پتانسیل توسط فعالیتهای متابولیکی که شرایط مطلوب خوردگی را القا میکند.( مثلا اثر آلودگی قارچی در سیستمهای سوختی/ آبی)
-4 تغییر شیب اکسیژن جهت ایجاد اختلاف دمشی مثلا اثر بیوفیلمهای هوازی باکتریها روی خوردگی فولاد زنگ نزن در آب دریا.
5- حمله انتخابی باکتریها در نواحی جوشکاری شده فلزات
6- تسهیل شروع حفره دار شدنPitting) )
توسط اثرات اتصال میکروبی ( مثلا شروع حفره دار شدن در نقا ط اتصال میسلیوم قارچی روی آلیاژهای آلومینیم).
تقریباً هیچ چیزی در جهان وجود ندارد که تعدادی از ارگانیسمها نتوانند آنرا تجزیه کنند و اساساً یکی از نقش های مفید میکروبها، پاکسازی محیط از طریق تجزیه مواد زائد و برقراری چرخه های زیستی از قبیل چرخه کربن، گوگرد و ... می باشد .
البته در برخی مواقع مواد و تجهیزات به طور نا خواسته مورد تجزیه بیولوژیکی قرار می گیرند و موجب افزایش هزینه های نگهداری و تعمیرات تجهیزات می شوند . نقش تجزیه کنندگی میکروارگانیسمها به قدری شگفت انگیز است که برخی از کشورها به فکر استفاده از قابلیت تجزیه بیولوژیکی به عنوان یک سلاح غیر کشنده ضد مواد و تجهیزات (ضد آمادی ) افتاده و تحقیقات فراوانی را در این زمینه انجام داده اند. یکی از برنامه های این کشورها موثر تر کردن قابلیت تجزیه بیولوژیکی توسط انجام تغییرات مهندسی ژنتیک روی میکروارگانیسمهای تجزیه کننده و افزایش کارایی آنها می باشد.
سوختها منابع کربنی فراوانی برای رشد میکروبی دارند اما در مواد تغذیه ای غیر آلی از قبیل نیتروژن، فسفر و پتاسیم فقیر هستند.
اولین نشانه های آلودگی میکروبی سوخت عبارتند از :
- گرفتگی فیلتر ها
- کم رسیدن و یکدست نبودن جریان سوخت
- متغیر شدن فشار احتراق
و افزایش نرخ سایش رینگهای پیستون و دیواره داخلی سیلندر و فولینگ انژکتور.
آلودگی میکروبی سوخت بصورت ایجاد کدورت در سوخت و ایجاد لجن خاکستری /قهوه ای در سطح مشترک آب و سوخت ظاهر می شود و درموارد آلودگی شدید و طولانی مدت، خوردگی ممکن است اتفاق بیفتد .
پیشگیری و رفع آلودگی میکروبی:
همانطور که ذکر شد، مشکلات میکروبیولوژیکی میتواند بسیار متعدد باشند که احتیاج به راهکارهای اختصاصی خودشان را دارند، اما اصول اساسی معین و مشترکی برای پیشگیری و رفع آلودگی میکروبی وجود دارند که ذکر میشوند:
پیشگیری فیزیکی:
پیشگیری فیزیکی عبارتست از جلوگیری از ورود میکروبها، بویژه آنهایی که هم اکنون با رشد در محیط مناسب سازگارشده اند.
از پخش شدن آلودگی توسط عبوردادن مایعات تمیز از لوله ها و فیلترهای آلوده و ورود آنها به مخزن های کثیف باید جلوگیری نمود. همچنین حضور آب و شرایطی که رشد میکروبی را تشویق میکند نیز باید محدود شود.
آلودگی زدایی فیزیکی:
ته نشین سازی، گرما، فیلتراسیون و روشهای سانتریفوژی همگی به رفع آلودگی کمک می کنند. انتخاب فرآیند به نوع وسیله و محدودیت زمانی بستگی دارد.
پیشگیری شیمیایی:
محافظت علیه آلودگی جزئی با استفاده از مواد نگهدارنده سوخت و روانکار جهت پیشگیری، ترجیحاً نسبت به رفع آلودگی، در طی مدت زمان طولانی و با عمل آهسته اما مداوم انجام میشود.
آلودگی زدایی شیمیایی:
طیف وسیعی از زیست کش (بیوسید) های شیمیایی برای این منظور در دسترس هستند . کشتن میکروبها توسط راههای شیمیایی مشکل نیست، اما ثابت شده است که تلاش برای انجام آن پر خطر است، مگر اینکه سازگار بودن بیوسید از نظرشیمیایی با سوخت مصرفی به اثبات رسیده باشد و ویژگی های فیزیکی آنها را تحت تاثیر قرار نداده ، اثرات نامطلوب دیگری نداشته باشد. در حالی که استفاده از بیوسیدهای اشتباه میتواند اثرات جبران ناپذیری ایجاد کند.
حتی بیوسید صحیح باید به دقت و در غلظت مناسب استفاده شود . استفاده در دوز کمتر مشکل را علاج نخواهد کرد و دوز بالا می تواند به خاطر ایجاد بخارات سمی، خطری برای سلامتی باشد . این ترکیبات همگی سمی هستند و باید تنها با رعایت ملاحظات بهداشتی، ایمنی و زیست محیطی استفاده شوند.
روش های جداسازی اولیه و تغلیظ :
- 1- استخراج: جهت تولید آنتی بیوتیک ها در مقیاس بزرگ
- 2- میکروفیلتراسیون
- 3- اسمز معکوس
- روش اصلی برای جداسازس محصولات بیولوژیکی : استخراج
روش های استخراج :
- استخراج ناپیوسته (Batch extraction )
- استخراج مرحله ای ( Stage extraction )
- استخراج دیفرانسیلی (Differential extraction )
- استخراج جزئی با یک فاز ساکن
(Fractional extraction with a stationary phase )
- استخراج جزئی با دو فاز متحرک
(Fractional extraction with two moving phase )
استخراج ناپیوسته (Batch extraction ) :
- در این نوع استخراج محلولی که حاوی ماده حل شونده مطلوب می باشد با یک حلال غیر قابل استخراج ، مخلوط می شود.
- محلول اولیه یک محلول رقیق آبی بوده و حلال غیر قابل استخراج، حلال آلی می باشد. ماده حل شونده در فاز جدید آلی حل می شود تا اینکه غلظت در دو فاز آبی و آلی به حالت تعادل برسد.
- حجم عملیات مشخص کننده وسیله مورد استفاده برای جداسازی است :
- مقیاس آزمایشگاهی : قیف جداکننده – دکانتور (Separatory Funnel )
- مقیاس صنعتی : جداکننده ها ( Separator )
بررسی استخراج ناپیوسته به دو روش امکان پذیر است :
1- تحلیلی
2- گرافیکی ( نموداری یا ترسیمی )
استخراج مرحله ای ( Stage extraction ) :
- وقتی بکار می رود که در یک استخراج تک مرحله ای جداسازی کافی صورت نگیرد و یا جزء بازیافت شده مناسب و به اندازه کافی نباشد.
- نکات مهم در این دستگاه ها :
1- اگر دو مایع خیلی زیاد مخلوط شوند ممکن است قطرات ریزی تشکیل شود که شدت استخراج را زیاد می کند ولی ته نشینی را به تاخیر می اندازد.
2- اگر دو مایع به مقدار خیلی کم مخلوط شوند قطرات درشتی را تشکیل می دهند که سطح کافی جهت استخراج سریع را نداشته ولی به سرعت جدا می شوند.
استخراج دیفرانسیلی (Differential extraction ):
- وقتی صورت می گیرد که یک مایع سنگین و یک مایع سبک به طور مداوم از روی یکدیگر عبور کنند. در این فرایند ماده حل شونده از یک فاز به فاز دیگر انتقال می یابد، اما شدت انتقال کافی نیست تا سامانه استخراج به حالت تعادل برسدکه نتیجه آن جداسازی قابل توجه محصول بدون زمان ته نشینی بالقوه سخت که مشخصه استخراج مرحله ای می باشد.
استخراج جزئی با یک فاز ساکن
(Fractional extraction with a stationary phase )
- در این روش یک فاز سبک که شامل چندین ماده حل شونده است با یکسری لوله که در ابتدا حاوی فاز سنگین خالص می باشد در تماس قرار می گیرد که نتیجه آن جداسازی و تخلیص بالقوه مواد حل شونده ای است که ابتدا در فاز سبک بوده اند.
- این روش در مقیاس نسبتا کوچک و انحصارا برای مواد بیولوژیک بکار می روند.
- این روش به نام مخترعش استخراج کریج ( Craig ) نیز نامیده می شود.
استخراج جزئی با دو فاز متحرک
(Fractional extraction with two moving phase )
- در استخراج جزئی با دو فاز متحرک دو ماده حل شونده هر دو فاز سنگین و سبک در جهت عکس یکدیگر حرکت می کند.
- در این نوع استخراج یک خوراک مداوم توسط دو حلال جاری در جهت متقابل صورت می گیرد.
- این نوع استخراج جزئی نه تنها ماده حل شونده موردنظر را جدا می کند بلکه آن را تخلیص نیز می کند.
تکنولوژیهای جدید برای جداسازی و تجزیه وتحلیل پروتین ها و اسیدهای آمینه
|
نقش پروتئین ها در رژیم غذایی |
پروتئین ها مواد مغذی اصلی هر سلول زنده هستند. در ساختمان آنها نه تنها کربن ، هیدروژن و اکسیژن وجود دارد، بلکه ازت و گاهی گوگرد نیز موجود می باشد.
پروتئینها مسئول انجام اعمال گوناگونی هستند. نقش آنها از تشکیل ماده انقباضی عضلات گرفته تا ساختن بعضی از هورمون ها، آنزیم ها و آنتی کورها، تبدیل انرژی شیمیایی به کار و انتقال اکسیژن و هیدروژن متنوع می باشد.
روش های جداسازي پروتئينها
جداسازي مخلوط هاي پروتئيني پيچيده با قدرت تفكيكي و قابليت تكرارپذير بالا, براي انجام موفقيت آميز پروتئوميكس بسيار پراهميت است. در ساليان اخير ترکيب الکتروفورز دو بعدي, طيف سنجي جرمي, و ابزار بيوانفورماتيک در مقياس بسيار وسيعي براي تحقيقات پروتئوميکس به کار گرفته شده است.
با استفاده ي گسترده از الکتروفورز دو بعدي, محدوديت هاي اين روش به تدريج مشخص شده اند. اين محدوديت ها عبارتند از:
1-با اين روش نمي توان پروتئین را به طور کامل آناليز کرد. پروتئين هاي ظاهر شده بر روي يک ژل فقط نماينده قسمتي از تمام پروتئين هاي موجود در نمونه هستند. به طور کلي آن پروتئين هايي که در ژل ظاهر مي شوند پروتئين هايي با فراواني بالا در نمونه هستند. پروتئين هايي که در تعداد نسخه هاي کم حضور دارند با روشهاي رنگ آميزي موجود نمايان نمي شوند. علاوه بر اين پروتئين هاي بسيار بزرگ, بسيار کوچک, بازي نيز در شرايط معمول آشکار نمي شوند.
2- يکي از مشکلات اصلي در الکتروفورز دو بعدي پروتئين هاي غشايي با هيدروفوبيسيته بسيار زياد هستند که در روشهاي محلول سازي رايج به صورت محلول در نمي آيند.
3-اتوماتيک کردن اين روش بسيار سخت است و به همين دليل روشي با ظرفيت آناليز زياد نيست.
براي رفع اين محدوديت ها, روشهاي ابداعي زيادي براي الکتروفورز دو بعدي ايجاد شده است.
براي مثال استفاده از 1-دترجنتهاي قوي تر,2- جزء به جزء کردن نمونه,3- استفاده از IPG با محدوده ي pH باريک, 4-رنگ هاي فلورسانت 5- روباتها براي بريدن و هضم آنزيمي ژل ها.
به علاوه پيشرفتهاي زيادي نيز در ابداع و توسعة روشهايي جايگزين براي جداسازي پروتئينها در پروتئوميكس بدست آمده است, اما هنوز هيچکدام نتوانسته اند جايگزين قابل رقابتي براي الكتروفورز دوبعدي باشند.
دليل اين امر خصوصيات ويژه ي اين روش است که عبارتند از:
- غناي اطلاعات نهفته در داده هاي بدست آمده از الکتروفورز دو بعدي - اطلاعات مختلفي از نقاط ظاهر شده بر روي ژل الکتروفورزبدست مي آيد. از جمله نقطه ي ايزوالکتريک, وزن مولکولي و کميت نسبی آن. در ترکيب با طيف سنجي جرمي هر نقطه را مي توان تعيين هويت نمود. با توجه به ظهور چندين نقطه بر روي يک ژل به حجم زياد اين اطلاعات مي توان پي برد.
- امکان جداسازي و تعيين پروتئين هاي با تغيير بعد از بیوسنتز - در اغلب مواقع, پروتئين هايي که بعد از ترجمه تغيير يافته اند به صورت دسته نقاطي که به صورت يک توده عمودي يا افقي هستند در ژل الکتروفورز دو بعدي ظاهر مي شوند. اين پروتئين هاي تغيير يافته به سهولت با طيف سنجي جرمي قابل تشخيص هستند.
- قابليت تفکيک زماني و مکاني مراحل آناليز پروتئین - مي توان الکتروفورز دو بعدي را در يک آزمايشگاه تحقيقاتي انجام داد و بعد از انتخاب نقاط پروتئيني مورد علاقه, آنها را در زماني ديگر در مرکزي خدماتي, تعيين هويت کرد. به علاوه ژلهاي خشک شده ي الکتروفورز دو بعدي را مي توان سالها نگاهداري کرد و سپس با طيف سنجي جرمي آناليز نمود. بدين ترتيب مي توان بايگاني کم حجم و پر ارزشي را در اختيار داشت.
- سهولت و ارزاني نسبي انجام آن در مقايسه با ديگر روشها از سهولت بسيار بيشتري بر خوردار است و اغلب آزمايشگاه ها با تکنيک هاي رايج الکتروفورز يک بعدي آشنايي دارند. همچنين قيمت تجهيزات و مواد در مقايسه با ديگر روشها بسيار ارزانتر است.
پيوست
پروتئوميكس: علمي كه به بررسي پروتئين هاي سنتز شده موجود زنده به عنوان منبع اطلاعات در مورد موجود زنده و نحوه ي سازوكار بدن آن مي پردازد.
شناسایی و جداسازی پروتئین ها و ملكولهای كوچك به كمك نانو حفره ها
نانو حفره ها قادر به جداسازی رشته های DNA یا داروهای با کاربرد درمانی از محلولها بر اساس اندازه حفره خود میباشند. یکی از محققان دانشگاه MIT نانو حفره هایی ایجاد کرده است که قادر است ملکولهای خاصی را شناسایی و با آنها واکنش دهد.
|
نانو حفره ها قادر به جداسازی رشته های DNA یا داروهای با کاربرد درمانی از محلولها بر اساس اندازه حفره خود میباشند. یکی از محققان دانشگاه MIT نانو حفره هایی ایجاد کرده است که قادر است ملکولهای خاصی را شناسایی و با آنها واکنش دهد
|
اسید آمینه
پروتئینها ، زنجیرههای خطی یا پلیمرهایی هستند که از ترکیب اسیدهای آمینه حاصل میشوند. اسید آمینهها ، حروف الفبایی پروتئینها را تشکیل میدهند و چون امکانات بالقوه نامحدودی در طرز توالی و طول زنجیره اسید آمینهها در تولید پروتئینها وجود دارد، از اینرو انواع بیشماری از پروتئینها نیز میتوانند وجود داشته باشند.
اختلاف هر اسید با سایر اسیدهای آمینه ، در زنجیره جانبی هر یک از اسیدهای آمینه است. اسیدهای آمینه در آغاز تشکیل زمین ، به همراه سایر مواد آلی پیدا شدند.
اسیدهای آمینهای که در حضور پرتوهای فرابنفش بوجود آمدند، گوناگونی بسیار داشتهاند. اما به دلایلی ناشناخته تنها بیست اسید آمینه ، آن هم از نوع L ، در یاخته زنده کاربرد پیدا کرد.
روشهای جداسازی اسیدهای آمینه از یکدیگر
مشتق سازي اسيدهاي آمينه
درجداسازي مشتقهاي اسيدهاي آمينه مي توان از روش هایی مانند جز به جز كردن اجزا سلولي , الكترو فورز در فازمايع , كروماتوگرافي جذبي ورسوب دهي انتخابي سود جست زيرا , اسيــدهاي آمينـه داراي فعاليت فلورسانس وماورابنفش نبوده ( بجز اسيــدهاي آمينه حلقوي نظير فنيل آلانين ) از اين رو براي آشكارسازي آنها بايد گروههاي شيميايي با چنين فعاليتي به آنها اتصال يابد .
اين مشتق سازي بعد از هيدروليز صورت مي پذيرد وممكن است قبل از جداسازي يا پس از آن انجام يابد . در مشتق سازي بعد از جداسازي براي جداساختن مخلوط اسيدهاي آمينه ازروش كروماتوگرافي تبـادل يوني بهره گرفته مي شود . در حاليكه در مشتق سازي قبل از جداسازي براي جداساختن مخلوط اسيدهاي آمينه از روش كروماتوگرافي فاز معكوس استفاده مي شود .
مشتق اسيدهاي آمينه وفنيل ايزوتيوسيانات با استفاده از روش كروماتوگرافــــي فاز معكوس براساس هيدروفوبيسيتي گروه R اسيد آمينه از يكديگر جدا ميشوندودر طول موج 254 نانومتر آشكارســـــازي مي شوند .
رسوب دهی
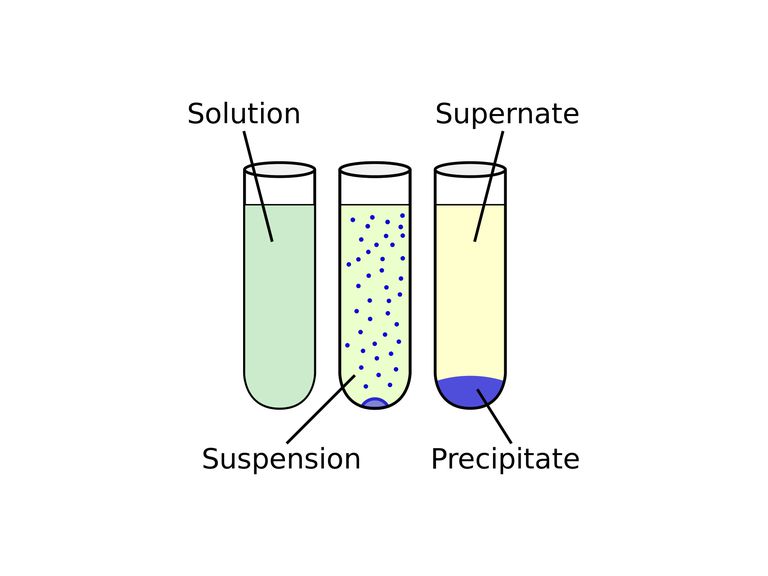
فرایند حذف جامد از یک محلول که یک روش مهم در خالص سازی پروتئین هاست.در پدیده رسوب دهی مطلوب است که از تشکیل دامنه وسیعی از ذرات با اندازه های مختلف جلوگیری شود. به طور کلی رسوب دهی یعنی کاهش قدرت حلالیت پروتئین که در اوایل فرآیند خالص سازی از آن استفاده می شود. هدف رسوب دهی کاهش حجم و افزایش غلظت است.
مزایای رسوب دهی:
- کم هزینه بودن روش
- قابلیت اجرا در سیستم پیوسته
- رسیدن به فرمی از پروتئین که اغلب دارای پایداری بالاست.
مراحل تشکیل رسوب:
اختلال اولیه
هسته زایی
رشد کنترل شده توسط پدیده نفوذ
رشد کنترل شده حرکت سیال
با مطالعه پدیده ی تشکیل رسوب امکان کنترل پارامترهای تاثیرگذار بر رسوب دهی پروتئین نهایی فراهم میشود.
مشخصات رسوب های پروتئینی:
توزیع اندازه ذرات
دانسیته
قدرت مکانیکیشدت ذرات رسوب کرده:
زمانی که ذرات رسوب کرده بواسطه ی کلوئیدی شدن و تجمع باهم , به اندازه کافی رشد نمایند آماده شکسته شدن در اثر برخورد می باشند.
شدت شکست ذرات
شدت تنش
غلظت ذرات
مدل جابجایی
یک مدل موفق برای توصیف فرایند شکست رسوبات پروتئینی.
سرعت تغییر اندازه رسوب به صورت تابعی از جابجایی از یک قطر تعادلی
روشهاي رسوب دهي:
در روشهاي آماده سازي نمونه ، رسوب دادن پروتئين ها به عنوان يک مرحله اختياري تلقي مي گردد . اين روش براي جدا کردن انتخابي پروتئين ها از مواد آلاينده و تداخل کننده در محلول مانند نمک ها ، دترجنت ها ، اسيدهاي نوکلئيک ، و غيره به کار گرفته مي شود . از اين روش براي تغليظ پروتئين هاي موجود در يک نمونه که در حالت عادي بسيار رقيق باشند ، نيز استفاده مي شود .
نکته: بايد توجه داشت که هيچ روش رسوب دهي به طور کامل کارامد نيست و برخي از پروتئين ها بعد از رسوب داده شدن ، مجددا محلول نمي شوند . به همين دليل بسته به هدف از انجام الکتروفورز دو بعدي استفاده کردن از اين روش را در دستور کار مي توان قرار داد .
در صورتيکه هدف از انجام الکتروفورز دو بعدي به دست آوردن کاملترين نمايه دو بعدي يک نمونه باشد ، بايد از انجام رسوبدهي صرف نظر کرد . جزء به جزء کردن نمونه (Fractionation):
پروتئين هايي که در بافتهاي اوکاريوتي بيان مي شوند ، از گوناگوني بسياري برخوردار بوده ، و داراي محدوده ديناميک (محدوده غلظت پروتئين هاي داخل يک نمونه بين کمترين تا بيشترين غلظت Range Dynamic وسيعي هستند) . برخي از مواقع در نمونه هايي اين چنين ، به منظور کاهش پيچيدگي نمونه و افزايش تعداد پروتئين هايي که داراي نسخه پايين هستند ، نمونه جزء به جزء مي شود جزء به جزء کردن نمونه (Fractionation):
پروتئين هايي که در بافتهاي اوکاريوتي بيان مي شوند ، از گوناگوني بسياري برخوردار بوده ، و داراي محدوده ديناميک (محدوده غلظت پروتئين هاي داخل يک نمونه بين کمترين تا بيشترين غلظت Range Dynamic وسيعي هستند) . برخي از مواقع در نمونه هايي اين چنين ، به منظور کاهش پيچيدگي نمونه و افزايش تعداد پروتئين هايي که داراي نسخه پايين هستند ، نمونه جزء به جزء مي شود
روشهاي جزء به جزء کردن ، ممکن است مزاياي بسياري در غني سازي پروتئين ها داشته باشند ، اما اصلي ترين نکته منفي در استفاده از اين روشها ، اين است که بسيار زمانگير و بسيار پيچيده اند . همچنين نمي توان در يک زمان چند نمونه را وارد اين مرحله از کار نمود . اما مزيت اصلي آن ،تعيين جايگاه پروتئين ها از نظر ساختماني در زير ساختار سلولي و تعيين عملکرد آنها است . استخراج پي در پي (Sequential Extraction):
پروتئين ها از يک سلول يا بافت بر اساس حلاليت آنها در دسته اي از بافر ها که قدرت و خاصيت محلول سازي آنها به تدريج افزايش پيدا مي کند ، روش ديگري از جزء به جزء کردن است . رسوب دهي به وسيله نمك :
روش عمومي براي انجام عمل رسوب دهي استفاده از نمك است كه با افزايش مقدار نمك حلاليت پروتئيني كم شده و به هم پيوسته و رسوب مي کند .
رسوب دهي به وسيله حلال هاي آلي :
با افزايش حلال آلي ، قدرت حلاليت مولكولهاي باردار آب دوست پروتئينها در محيط آبي كم شده و باعث به هم پيوستن ذرات مولكولي و رسوب دهي آنها مي شود . ( مانند مكانيزم رسوبدهي پروتئين ها در نقطة ايزوالكتريك , در غلظتهاي پايين نمك) .
به عنوان مثال اتانل , در جداسازي پروتئينهاِي پلاسمايي بسيار مورد استفاده قرار ميگيرد .
رسوب دهي به وسيله پليمرهاي آلي :
اين روش , مانند روش استفاده از حلال آلي و از طريق كاهش فعاليت محيط آبي است. به عنوان مثال Poly Ethylen Glycol , در جداسازي پروتئينهاِي پلاسمايي , فراوان مورد استفاده قرار ميگيرد . تشکیل ته نشینی با ورود یک جامد دریک محلول و انجام واکنش شیمیایی با نفوذ محلول در جامد است.
مواد شیمیایی که باعث شکلگیری جامد هستند رسوب نام دارند.اما اگر نیروی کافی به ذرات جامد نرسد رسوب در تعلیق باقی می مانند.پس از شکلگیری رسوب به ویژه هنگامی که با استفاده از سانترفیوژ به توده فشار میرسد ممکن است به شکل گلوله درآید.
مایعی که بالای مواد جامد ته نشین شده باقی مانده لایه شناور یا رویی نامیده می شود.
ته نشینی ممکن است در یک محلول فوق اشباع سریعتر رخ دهد.
در شیمی ته نشینی مواد و ایجاد رسوب به صورت طبیعی راco-precipitation یا (CPT) می گویند.که یک مسأله مهم در تجزیه و تحلیل شیمیایی است.
co-precipitation اغلب نا مطلوب است اما در برخی موارد می تواند مورد استفاده قرار گیرد,در وزن سنجی تجزیه و تحلیل که شامل تسریع تجزیه و اندازه گیری جرم آن برای تعیین غلظت وخالصی .
از طرفی یک مشکل است زیرا به دلیل نا خالصی های نا مطلوب یه توده اضافی است.
جذب سطحی
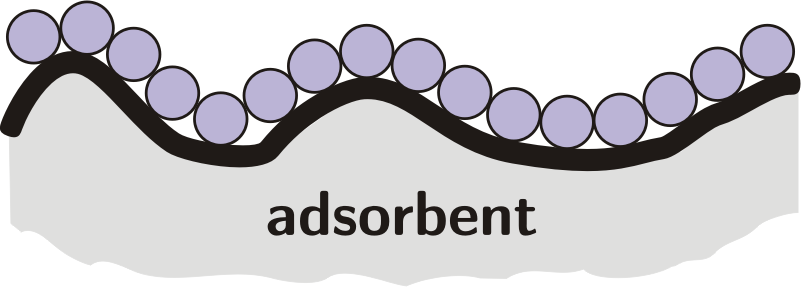
درعملیات جذب سطحی انتقال یک جزء از فاز گاز یا مایع به سطح جامد صورت می گیرد.
واژه جذب سطحی برای تشریح این حقیقت بکار می رود که غلظت مولکول های جذب شده در سطح تماس جامد بیشتر از فاز گاز یا محلول است. جذب روی یک سطح جامد به علت نیروی جاذبه اتم ها یا مولکول ها در سطح آن جامد است. در عمل جذب سطحی نیروهای مختلفی اعم از فیزیکی و شیمیایی مؤثرند و مقدار آن بستگی به طبیعت ماده جذب شده و جسم جاذب دارد و به این دلیل می توان مثلا ماده ای را که در یک مخلوط وجود دارد جدا نمود.
جذب سطحی نیازمند جاذب است.یک ماده جامد که جز حل شده مورد نظر بتواند به صورت برگشت پذیر روی ان جذب شود.
در ادامه در موری خصوصیات جاذب بحث خواهد شد.
جامدی که بر روی سطح آن جذب اتفاق می افتد جاذب یا سوسترا می نامند. مایع جذب شده را مجذوب می نامند. جذب سطحی بر روی سطح مشترک جامد مایع به وقوع می پیوندد.
جامد های جاذب معمولا به شکل گرانول (ذرات کروی شکل با قطر چند میلیمتر) مصرف می شوند و اندازه آن ها از 12 میلیمتر قطر تا 50 میکرومتر متغیر است. جامد ها باید بر اساس کاربرد و موقعیت مصرف دارای بعضی خواص مهندسی باشند. برای مثال اگر از آن ها در یک بستر ثابت با جریان گاز یا مایع استفاده می شود، نباید اختلاف فشار زیادی ایجاد کنند و همچنین نباید توسط جریان سیال به خارج حمل شوند. آن ها باید از مقاومت و سختی خوبی برخوردار باشند تا در اثر حمل و نقل و همچنین در اثر وزن خود در بستر خرد نشوند. در صورتی که بخواهیم آن ها را از ظروف نگهداری به داخل و خارج انتقال دهیم، باید به راحتی جریان پیدا کنند.
چند مثال که در ادامه بیان شده است نمایانگر طبیعت عمومی جداسازی ها
خواهد بود و کاربرد های اصلی آن را نشان می دهد.
در حالت جداسازی های گازی از فرایند جذب، در رطوبت زدائی ها هوای خشک و دیگر گازها، بوزدائی و جداسازی ناخالصی ها از گازهای صنعتی مثل دی اکسید کربن، بازیابی حلال های پر ارزش از محلول رقیق آن ها با هوا یا گاز های دیگر، و جداسازی مخلوطی از هیدرو کربن های گازی مانند مخلوطی از متان، اتیلن، اتان، پروپیلن و پروپان استفاده می شود.
از فرایند های جداسازی مایع می توان رطوبت زدائی بنزین، رنگ زدائی محصولات نفتی و محلول های آبکی قندی، بوزدائی و طعم زدائی آب، و جداسازی هیدرو کربن های آروماتیکی و پارافینی، را نام برد. که هر کدام از این موارد در صنعت کاربرد وسیعی داشته و بنا به مورد و شرایط محدوده کاری از آن استفاده می شود.
سطح تماس
غلظت
دما
نوع ماده جذب شده و جاذب
حالت ماده جذب شده و جاذب
با افزایش سطح تماس مقدار جذب افزایش می یابد، بهترین جذب کننده ها موادی هستند که ذرات ریزتری داشته باشند و به عبارت دیگر سطح تماس بیشتر داشته باشند. از میان مهمترین جذب کننده ها می توان ژل، سیلیس، کربن اکتیو را نام برد.
مقدار ماده جذب شده برای واحد جرم جذب کننده تابعی از غلظت ماده حل شده می باشد. بررسی این دو کمیت در دمای ثابت منجر به بدست آوردن کمیت ایزوترم جذب سطحی می شود. این ایزوترم ها توسط افراد مختلفی بررسی شده است که مهمترین آن ها ایزوترم فرندلیش می باشد.
افزایش دما اصولا باعث کاهش جذب سطحی می شود مگر در مواردی که جذب سطحی همراه با واکنش شیمیایی باشد.
نوع ماده جذب شده و جاذب در جذب سطحی تأثیر گذار است به طوری که بعضی از مواد جاذب قدرت جذب زیاد نسبت به ماده حل شده به خصوصی از خود نشان می دهند، در حالی که نسبت به ماده دیگر قدرت جذب کمتری دارند.
حالت ماده جذب شده و جاذب، همراه بودن آن با واکنش شیمیایی، برگشت پذیر بودن و یا برگشت پذیر نبودن واکنش آن ها نیز در جذب سطحی تأثیر گذار است.
تا کنون مدل های ریاضیاتی گوناگونی به منظور بررسی فرایند جذب سطحی مورد استفاده قرار گرفته است در بین تمامی مدلهای ایزوترمی ارائه شده سه مدل فروندلیخ (Freundlich ) ،لانگمیر(Langmuir )و BET به طور گسترده تری مورد استفاده قرار می گیرند.مدل ایزوترمی فروندلیخ یک مدل تجربی (Emprical ) است در حالی که مدل لانگمیر و مدل BET دارای اساس تئوری(Theorical ) می باشند. ایزوترم لانگمیر بر مبنای مدل جذب تک لایه ای (Monolayer adsorption ) و ایزوترم BET برمبنای مدل جذب چند لایه ای (Multiple adsorption) می باشند.
برای بدست آوردن ایزوترم های جذب سطحی برای یک ماده جذب شونده بایستی مقدار مشخصی از ماده جذب شونده را در یک حجم ثابت از محلول نگه داشته و آنچه که تغییر می دهیم مقادیر کربن فعال باشد. بطور معمول در این حالت بیش از 10 ظرف لازم خواهد بود و زمانی که از کربن فعال پودری استفاده می شود، حداقل زمانی که مجاز است تا نمونه به تعادل برسد 7 روز می باشد. زمانی که از کربن فعال گرانوله استفاده می شود می باید آنرا پودر کنیم تا زمان های جذب سطحی را به حداقل برسانیم. در پایان تست مقدار ماده جذب شونده که در داخل فاز محلول باقیمانده است اندازه گیری می شود. مقدار ماده جذب شونده که به ازای واجد جرم ماده جاذب جذب شده است با استفاده از فرمول زیر محاسبه می گردد و به منظور بدست آوردن ایزوترم های جذب سطحی استفاده می شوند.
(Metcalf & Eddy, 2003).
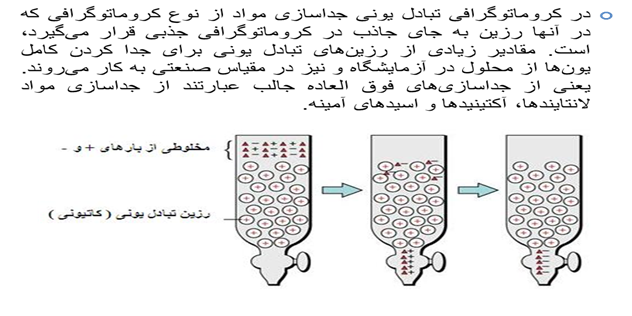
پديده تبادل يوني
فرایند تبادل یونی یکی از اشکال پدیده جذب سطحی است، که در آن فاز سیال در تماس با فاز جامد جاذب قرار میگیرد.فرآيند واكنش شيميايي بين يون هاي داخل فاز مايع و يون هاي فاز جامد مي باشد. يون هاي خاصي در داخل مايع ترجيحاً توسط مبدل يوني جامد جذب مي شود و به خاطر اين كه بايد حالت خنثاي الكتريكي برقرار گردد، مبدل جامد يون هايي را به داخل مايع آزاد كرده كه جايگزين يون هاي جذب شده گردد. فرآيند تبادل يوني به طور عمده در نرم سازي آب، حذف مواد معدني، نمك زدايي، حذف نيتروژن به كار مي رود.
تعادل مبادله یون به وسیله ی ایزوترم تبادل یون مشخص میشود.
ایزوترم تبادل یون از رسم )Azنسبت یونی معادل یون متقابلAدر مبادله گریون) بر حسب As(نسبت یونی معادل در محلول)در یک غلظت کلی ثابت ودرجه حرارت مشخص به دست می اید.
به اندرکنش های شیمیایی خاص بین ماده حل شونده و رزین بستگی دارد.جاذب از دو بخش حامل و لیگاند تشکیل شده است بدین صورت که یک لیگاند به صورت کوالانسی یا یونی به پایه متصل است.
جذب سطحی با یک بر خورد شیمیایی بین ماده حل شونده و لیگاند انجام میگیرد و هیچگونه جذبی توسط پایه انجام نمیگیرد.
جذب سطحی مواد حل شونده به طور انتخاب گر توسط لیگاند صورت میگیرد.
به عنوان مثال می توان به جذب سطحی انتی بادی ها توسط انتی ژن(به عنوان لیگاند) /جذب سوبسترا با انزیم تثبیت شده /جذب توالی خاصی از اسید نوکلییکها اشاره کرد.
از این نوع فرایند بیشتر در ازمایشگاهها استفاده میشود و کاربرد کمی در صنعت دارند.
در جذب سطحی ناپیوسته جاذب و سیال در یک محیط بسته (سیال وارد یا خارج نمیشود) در کنار هم قرار میگیرند.پس از طی شدن زمان مناسب برای جذب ماده مورد نظرفرایند به پایان میرسد.
این فرایند به دو محدودیت اساسی تعادل ترمودینامیکی و موازنه جرم بستگی دارد.محدودیت تعادل همان ایزوترم جذب است.
این قبیل مخازن در پاره ای از اوقات راکتور های پیوسته مجهز به همزن یا cstr نامیده میشود.
هنگامی که جدا سازی در مقیاس بزرگ مدنظر باشد معمولا از این دسته از فرایندها بیشتر از جذب سطحی ناپیوسته استفاده میشود.
روش انجام این جذب سطحی پیوسته بدین صورت است که :خوراک
به صورت پیوسته وبا دبی و غلظت ثابت وارد میشود.در ابتدا تانک حاوی حلال خالص وجاذب استفاده نشده می باشد.غلظت جز حل شده بر روی جاذب با زمان تغییر می کند.جریان خروجی از تانک به صورت پیوسته خارج میشود. اما غلظت ان با زمان تغییر میکند. از انجایی که عمل اختلاط و هم زدن در این مخزن به خوبی انجام میشودغلظت درون مخزن با جریان خروجی برابر است.
معمولا ازمایشات در تانکهای کوچک صورت گرفته و اطلاعات حاصل جهت طراحی در مقیاس بزرگتر به کار می رود.
جذب در بسترهای ثابت عمومی ترین و مهمترین نوع فرایند جدا سازی جذب سطحی مواد حل شونده میباشد.بستر ثابت به سادگی متشکل ازیک ستون پرشده باذرات جاذب می باشد.جریان حاوی ماده حل شده از یک طرف وارد واز طرف دیگر خارج می شود.در ابتدا بیشتر ماده حل شده جذب میشود بطوریکه غلظت حل شونده در خروجی پایین است.ولی با ادامه فرایندجداسازی غلظت خروجی ابتدا به کندی و سپس به طور ناگهانی افزایش یافته و فرایند جذب متوقف می شود.سپس ماده جذب شده با شست وشوی بستر با اب درphهای مختلف یا با حلالهای مختلف شسته می شود.
کروماتوگرافی
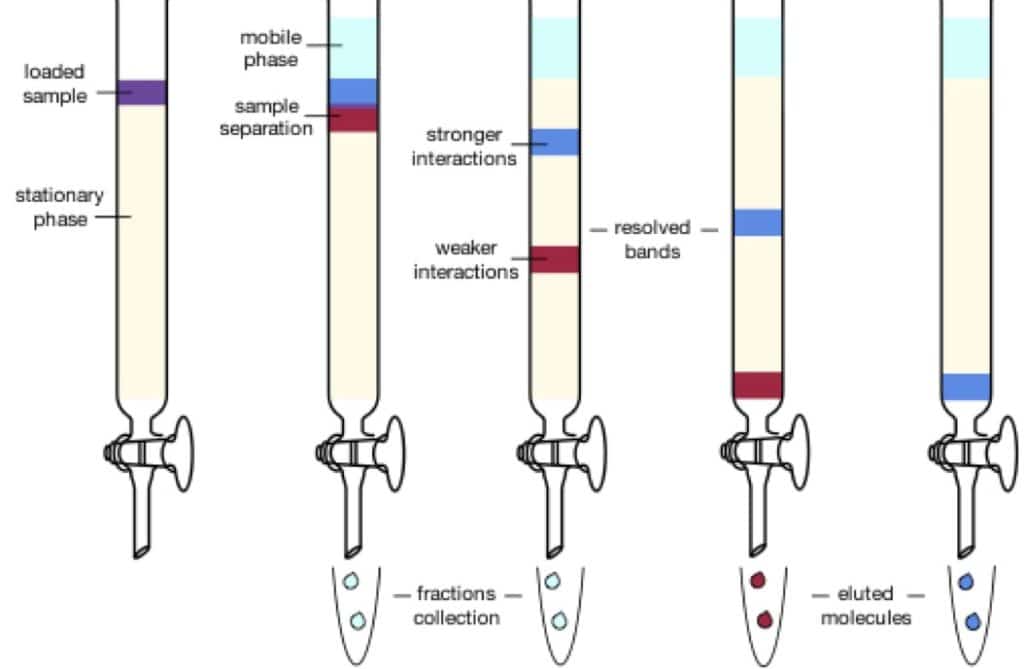
پر کاربردترین شیوه جداسازی مواد تجزیهای کروماتوگرافی است که در تمام شاخههای علوم کاربردهایی دارد. کروماتوگرافی گروه گوناگون و مهمی از روشهای جداسازی مواد را شامل میشود و امکان میدهد تا اجزای سازنده نزدیک به هم مخلوطهای کمپلکس را جدا ، منزوی و شناسایی کند بسیاری از این جداسازیها به روشهای دیگر ناممکن است.
کروماتوگرافی متکی بر حرکت نسبی دو فاز است ولی در کروماتوگرافی یکی از فازها بدون حرکت است و فاز ساکن نامیده میشود و دیگری را فاز متحرک مینامند. اجزای یک مخلوط به وسیله جریانی از یک فاز متحرک از داخل فاز ساکن عبور داده میشود. جداسازیها بر اساس اختلاف در سرعت مهاجرت اجزای مختلف نمونه استوارند.[1]
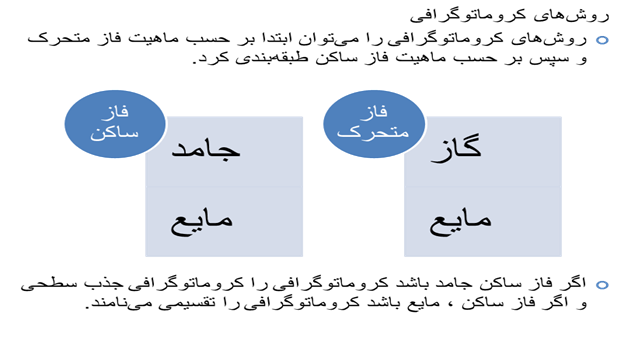
طبقه بندی گروماتوگرافی
- مایع ـ جامد
کروماتوگرافی جذب سطحی کروماتوگرافی تبادل یونی کروماتوگرافی لایه نازک کروماتوگرافی ژلی
- مایع - مایع: کروماتوگرافی تقسیمی کروماتوگرافی کاغذی
- گاز - جامد
- ستون کروماتوگرافی جذب سطحی
برای جداسازی مواد یک مخلوط ، میتوان از ستون استفاده کرد. داخل این ستون با جامد فعالی مانند آلومین (فاز ساکن) پر شده است و با حلالی مانند هگزان (فاز متحرک) پوشیده شده است. هرگاه نمونه کوچکی از مخلوط در بالای ستون قرار گیرد ، نواری از ماده جذب شده تشکیل میشود، حلال با عبور خود از میان ستون اجزای مخلوط را با خود حمل میکند.
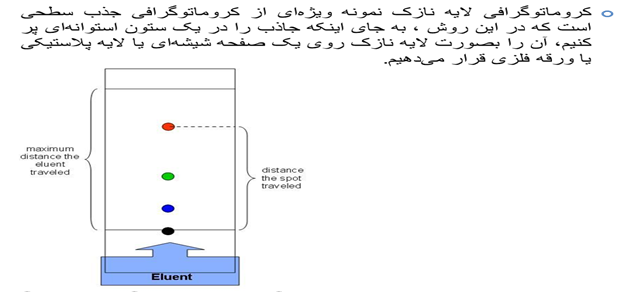
- ژل کروماتوگرافی
- در مطالعات جذب سطحی بر روی سیلیکاژل و کربن فعال ، اثرات الک مولکولی با موادی که جرم مولکولی بالایی دارند، مشاهده شده است. جداسازیهای مبتنی بر الک کردن مولکولی را میتوان بر روی اجسام بیبار در جریان مهاجرت الکترو اسمزی از داخل ژلها انجام داد. این اساس جداسازیهایی را که مبتنی بر اندازههای نسبی مولکولها هستند، تشکیل میدهند و از اصطلاح صاف کردن بوسیله ژل استفاده میشود.
- انتخاب بهترین روش کروماتوگرافی
- انتخاب نوع روش کروماتوگرافی بجز در موارد واضح (مانند کروماتوگرافی گازی در جداسازی مواد گازها) عموما تجربی است. زیرا هنوز هیچ راهی جهت پیش بینی بهترین روش برای جداسازی مواد اجسام مگر در چند مورد ساده وجود ندارد. در ابتدا روشهای سادهتر مانند کروماتوگرافی کاغذی و لایه نازک امتحان میشوند. زیرا این روشها در صورتی که مستقیما قادر به جداسازی مواد نباشند نوع سیستم کروماتوگرافی را که جداسازی مواد بوسیله آن باید صورت بگیرد، مشخص میکنند آنگاه در صورت لزوم از روشهای پیچیدهتر استفاده میشود. [1]
مزیت روشهای کروماتوگرافی
ـ با روشهای کروماتوگرافی میتوان جداسازیهایی را که به روشهای دیگر خیلی مشکل میباشند انجام داد. زیرا اختلافات جزئی موجود در رفتار جزئی اجسام در جریان عبور آنها از یک سیستم کروماتوگرافی چندین برابر میشود.
- ـ مزیت کروماتوگرافی نسبت به ستون تقطیر این است که نسبتا آسان میتوان به آن دست یافت با وجود اینکه ممکن است چندین روز طول بکشد تا یک ستون تقطیر به حداکثر بازده خود برسد ولی یک جداسازی مواد کروماتوگرافی میتواند در عرض چند دقیقه یا چند ساعت انجام گیرد.
- ـ یکی از مزایای برجسته روشهای کروماتوگرافی این است که آنها آرام هستند. به این معنی که احتمال تجزیه مواد جداشونده به وسیله این روشها در مقایسه با سایر روشها کمتر است.
- ـ مزیت دیگر روشهای کروماتوگرافی در این است که تنها مقدار بسیار کمی از مخلوط برای تجزیه لازم است به این دلیل روشهای تجزیهای مربوط به جداسازی مواد کروماتوگرافی میتوانند در مقیاس میکرو و نیمه میکرو انجام گیرند.
- گاز کروماتوگرافی
- GC براي شناسايي و تعيين مقدار گاز انجام مي شود.
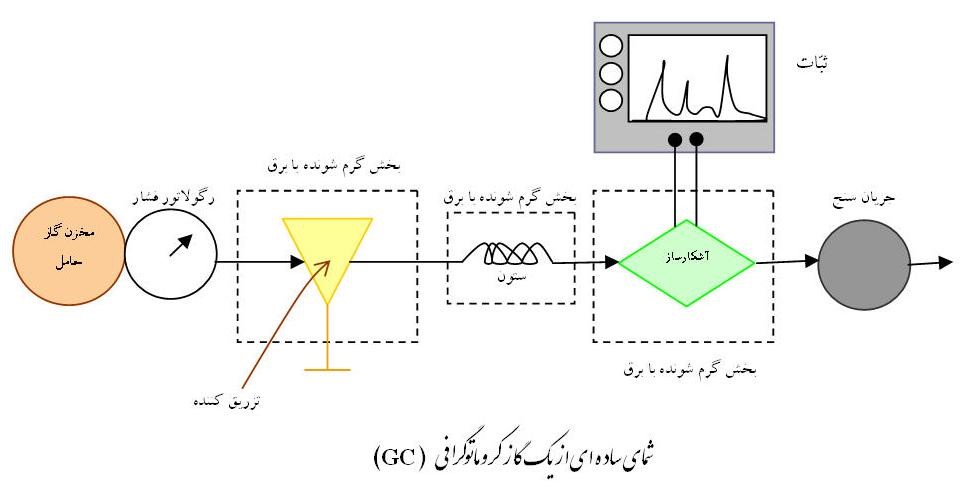
- ابتدا نمونه را توسط سرنگ داخل injector تزريق مي كنيم. نمونه پس از ورود به injector به بخار تبديل شده و با فاز متحرك مخلوط شده، وارد ستون مي شود. نمونه جذب ستون مي شود و در زمانهاي مختلف به وسيله گاز بي اثر از ستون بيرون مي آيد و وارد دتكتور مي شود. ستون قلب دستگاه است زيرا عمل اصلي كه جداسازي است در آنجا انجام مي شود. دتكتور شناسايي را انجام مي دهد جهت شناسايي مواد با GC از (Rt) Retention time استفاده مي شود. Rt زماني است كه طول مي كشد تا جسم از دتكتور بيرون بيايد ،يعني از زمان تزريق نمونه تا زمان ظاهرشدن پيك ها روي دستگاه كه براي يك ماده تحت شرايط ثابت، مقداري ثابت است. بنابراين از مقايسه Rt معلوم با Rt مجهول، مي توان اجزاي موجود در مجهول را تشخيص داد.
- آنالیز فرآیندهای کروماتوگرافی
- مدل تعادلی
- توزیع تعادلی یک مولکول مابین دو فاز که به دما بستگی دارد می تواند توسط یک معادله ساده توصیف شود. توزیع تعادلی در یک دمای مشخص ، ایزوترم نامیده می شود. ساده ترین فرم ، ایزوترم خطی است که توسط معادله زیر بیان می شود.
- K=x / y
- جائیکه K ثابت تعادلی ترمودینامیکی ،X غلظت در فاز متحرک و Y غلظت در فاز ساکن است.
- مدل آماری گوسی
- گیدینگ استفاده از معادله توزیع احتمالات گوسی را برای توصیف پیک های حاصل از کروماتوگرافی پیشنهاد داد .در یک سیستم کروماتوگرافی طراحی شده ، رسیدن به توزیع گوسی امکان پذیر است. توزیع زمان ماند مولکول ها در ستون منعکس کننده اختلافات موجود در مسیر طی شده توسط هر مولکول از ستون است. [4][5]
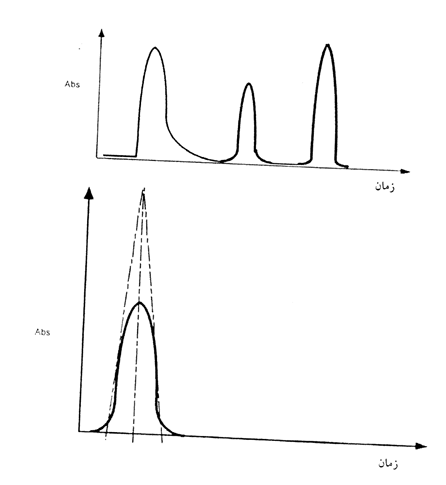
پیک های معمول کروماتوگرافی و پیک های گوسی
- مدل مرحله ای
این مدل نحوه توزیع حل شونده بین فاز متحرک و فاز ساکن در ستون را توصیف می کند. در این مدل ستون به جندین مرحله تقسیم می شود که در هر مرحله فاز متحرک با فاز ساکن در تعادل است.[1][5]
دو مکانیسم اصلی در کروماتوگرافی عبارتند از:[7]
کروماتوگرافی بر پایه مکانیسم جذبی.
کروماتوگرافی بر اساس مکانیسم غیر جذبی.
انواع روش های کروماتوگرافی:
وجود اندرکنش های مختلف همچون:اندرکنش های یونی،آب گریز،اندر کنش های اختصاصی و اندر کنش های بر پایه اندازه نمونه باعث بوجود آمدن روش های کروماتوگرافی مختلف شده است.[6]
1-کروماتوگرافی تبادل یونی
2-کروماتوگرافی فاز معکوس
3-کروماتوگرافی تمایلی
4-کروماتوگرافی ژل فیلتراسیون
تئوری کلی کروماتوگرافی:
بطور کلی کروماتوگرافی بر اساس توزیع مولکول های نمونه،بین دو فاز در ارتباط با هم پایه گذاری شده است. برای مثال در کروماتوگرافی جذبی،نمونه ی در حالت تعادل در فاز سیال،در زمان ارتباط با یک فاز ساکن(ماتریکس)،با توجه به تمایل نمونه برای جذب به فاز ساکن،بین دو فاز توزیع می گردد.
مولکول های با تمایل بیشتر برای جذب در فاز ساکن دارای غلظت بیشتر در فاز ساکن می شوند و مهاجرت آنها در ستون توسط فاز سیال آهسته تر خواهد شد و بر عکس نمونه های با تمایل کمتر نسبت به فاز ساکن،دارای غلظت بیشتری در فاز متحرک بوده و سریعتر در ستون حرکت می کنند[5]
قدرت تفکیک:
بدون شک مهم ترین پارامتر در کروماتوگرافی قدرت تفکیک است.قدرت تفکیک کیفیت جداسازی است بطوریکه قدرت تفکیک بالاتر به معنی هم پوشانی کمتر بین نمونه ها و خلوص بیشتر است.
فاکتورهای تاثیر گذار بر قدرت تفکیک:
فاز متحرک
مقدار نمونه
فاز ساکن
فاز متحرک:
قبلا اشاره شد که در کروماتوگرافی دو فاز متحرک و ساکن وجود دارد که فاز متحرک از روی فاز ساکن تثبیت شده عبور می کند.[7]
مهمترین عوامل مربوط به فاز متحرک عبارتند از:
دما : تغییرات دمای فاز متحرک افزایش گرانروی فاز متحرک مانع انتقال جرم بین دو فاز
افزایش دما کاهش نفوذ پذیری پروتئین ها و کاهش انتقال مولکول ها بین دو فاز
|
pH |
تغییر دما تغییر محیط (بویژه محیط های آبی بافری)
شدت جریان : کیفیت جداسازی و قدرت تفکیک...بیشترین قدرت تفکیک زمان به تعادل رسیدن دو فاز
برای عملکرد بهتر،باید فرآیند بجای سرعت زیاد در دمای محیط، با سرعت کم در دمای پایین تر انجام پذیرد.
وانسک و رگنیر گزارش دادند که با کاهش دما از 25درجه به 4 درجه سانتیگراد راندمان کار به میزان 40% افزایش یافته است.
همچنین به این نتیجه رسیدند که قذرت تفکیک متناسب با شدت جریان نیست و کاهش مداوم شدت جریان منجر به افزایش قدرت تفکیک نمیشود.
با کاهش شدت جریان مدت زمان انجام فرآیند جداسازی افزایش می یابد.لذا همیشه یک حد بهینه برای کاهش شدت جریان وجود دارد.
مقدار نمونه:
غلظت بالای نمونه باعث کاهش قدرت تفکیک می شود.نمونه های پروتئینی معمولا با غلظتی بین 4-0.5 میلی گرم بر میلی لیتر ستون تزریق می شوند،اگرچه در کروماتوگرافی تولیدی تا بیش از 10میلی گرم بر میلی لیتر ستون نیز افزایش می یابد.اگر ویسکوزیته نمونه بطور قابل توجهی از گرانروی محلول الوشن متفاوت باشد توزیع یکنواخت نمونه در ستون بسختی قابل اجراست .[4]
فاز ساکن:
پارامترهای فاز ساکن همچون شکل ذرات،اندازه ذرات ،توزیع اندازه ذرات،قطر روزنه ها،توزیع قطر روزنه ها،ظرفیت فاز ساکن،سطح فاز ساکن،حجم روزنه ها و فعالیت سطحی(پیوند های اختصاصی و غیر اختصاصی)بر قدرت تفکیک تاثیر می گذارند [.
ژل های مورد استفاده در کروماتوگرافی فاز معکوس:
ژل کروماتوگرافی فاز معکوس شامل دو قسمت اصلی ماتریکس پایه و لیگاندهای متصل به ماتریکس پایه می باشد،ماتریکس پایه باید از لحاظ شیمیایی و مکانیکی دارای پایداری باشد.
پارامترهایی مثل ترکیب شیمیایی ماتریکس پایه،اندازه ذرات،نوع لیگاندهای تثبیت شده،دانسیته لیگاندها در سطوح ذرات و اندازه روزنه های موجود در ذرات از مهم ترین پارامترهای تعیین کننده کارایی ژل های کروماتوگرافی فاز معکوس می باشد] 4-6[.
لیگاندهای مورد استفاده در کروماتوگرافی فاز معکوس:
انتخابیت در ژل های فاز معکوس قویا به نوع لیگاند متصل به ماتریکس پایه بستگی دارد.معمولا از هیدروکربن های زنجیره ای خطی(الکیلهای نرمال) بعنوان لیگاند در کروماتوگرافی فاز معکوس استفاده می شود.
لیگاندهای با زنجیره های الکیل با هشت کربن و یا کمتر،به دلیل نیاز به غلظت پایین تر حلال آلی برای الوشن کمترین زیان را به ساختمان پروتئین ها و پپتید ها می رساند.
علاوه بر ساختار لیگاند،دانسیته لیگاند بر سطح ژل های سیلیکا نشان داده که بر روی انتخابیت ژل تاثیر می گذارد
پارامترهای مهم در کروماتوگرافی فاز معکوس:
ارتفاع ستون:
تفکیک ماکرومولکول ها در کروماتوگرافی فاز معکوس نسبت به مولکول های آلی کوچک حساسیت کمتری به ارتفاع ستون دارد.و مولکول های بزرگ می توانند در ستون های کوتاه تفکیک شوند و معمولا افزایش ارتفاع ستون،قدرت تفکیک را بهبود نمی دهد.در حالی که تفکیک مولکول های کوچک همچون پپتید های با وزن مولکولی پایین با افزایش طول ستون بهبود می یابد
شدت جریان:
شدت جریان یک عامل مهم در تفکیک مولکول های کوچک همچون پپتید هاست اما مولکول های زیستی بزرگ همچون پروتئین ها به شدت جریان حساس نیستند.
شدت جریان های پایین نوعا در ستون های بلند ممکن است باعث کاهش قدرت تفکیک شود.
دما:
دما تاثیر زیادی در کروماتوگرافی فاز معکوس مخصوصا برای مولکول های با وزن مولکولی پایین همچون پپتید های کوتاه و اولیگونوکلئیک ها دارد.
فاز متحرک:
ترکیب شیمیایی فاز متحرک در کروماتوگرافی فاز معکوس معمولا شامل حلال های آلی و محلول با قطبیت پایین است.قطبیت پایین فاز متحرک باعث افزایش قدرت فاز متحرک در فرآیند الوشن ستون می شود.
استونیتریل و متانول از مهم ترین حلال های آلی هستند که مورد استفاده قرار گرفته اند.البته از ایزوپروپانول به دلیل قدرت الوشن بیشتر نیز استفاده شده است اما این حلال دارای گرانروی بالا می باشد که باعث افت کارایی و افزایش فشار برگشتی می شود.
همچنین بارداری پپتید ها در پروتئین ها در کروماتوگرافی فاز معکوس می تواند با تغییر pH فاز متحرک به دلیل وجود گروههای قابل یونیزه،تغییر نماید.درجه یونیزاسیون به pH فاز متحرک بستگی دارد.
pH فاز متحرک معمولا توسط اسید های قوی همچون تری فلورو استیک اسید تنظیم می شود.این اسید ها از یونیزاسیون گروه های اسیدی موجود در مولکول های حل شونده ممانعت می کنند.
گرادیان:
الوشن گرادیانی معمولا در جداسازی بیوملکول ها توسط روش کروماتوگرافی فاز معکوس استفاده می شود که معمولا دو جزیی و خطی است.البته از نوع گرادیان محدب یا مقعر در جداسازی های آنالیتیکال برای تفکیک چندین نمونه مختلف استفاده می شود. شکل گرادیان،شیب گرادیان و حجم گرادیان در کروماتوگرافی فاز معکوس اهمیت دارد. معمولا در جداسازی نمونه های کمپلکس در ابتدا از یک گرادیان با شیب غلظت پهن و بعد از تعیین شرایط اولیه،گرادیان به منظور تفکیک محصول مورد نظر تغییر داده می شود .شیب گرادیان معمولا با تغییر ترکیب درصدBدر واحد زمان یا در واحد حجم گزارش می شود.قدرت تفکیک متاثر از حجم گرادیان است. [1]
الکتروفورز
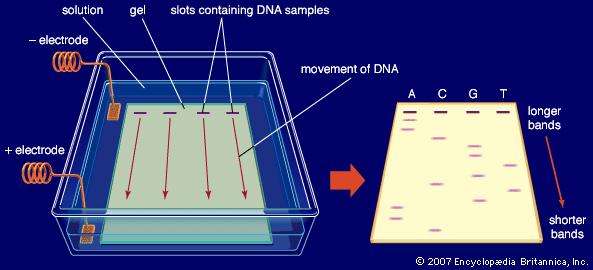
مقدمه
الکتروفورز اولین بار در سال 1937توسط یک شیمیدان سوئدی به نام تیسلیوس که بر روی پروتئین های سرم کار می کرد معرفی شد. در آن زمان به این کار روش مرز متحرک گفته می شد. در این روش مولکول ها ر اباید باردار کرد تا بر اساس میزان حرکتشان در یک میدان الکتریکی از هم جداشوند.در این صورت یون های مثبت به سمت الکترود منفی (کاتد) و یون های منفی به سمت الکترود مثبت (آند) مهاجرت می کنند.مولکول های بی بار هم بی حرکت باقی می مانند.بار بیشتر و اندازه کوچکتر منجر به مهاجرت سریع تر می شود.در الکتروفورز نیاز به یک بافر داریم که در بستر جامد مانند کاغذ ویا ژل نیمه جامد نگه داشته می شود و باعث رسانایی جریان الکتریکی که توسط ولتاژخارجی اعمال می شود,می گردد[11]
مهم ترین روش های باردارکردن استفاده از :
- اسیدها و بازها
- حلال های قطبی برای تفکیک یون ها
- تشکیل پیوندهیدروژنی
- قطبی شدن و تشکیل زوج یون
کاربرد اصلی الکتروفورز
- جداسازی
- ایزوله کردن
- خالص سازی مقادیر کم ترکیبات
برای مقایسه سیستم های مختلف این تکنیک از تحرک یونی استفاده می کنند.
انواع متداول الکتروفورز
۱)الکتروفورز سطحی : از یک نوار کاغذی یا استات سلولزی بعنوان فاز ثابت استفاده می شود. دو روش فوق جز در برخی کارهای پژوهشی کاربرد چندانی ندارند.
۲)الکتروفورز ژل : از یک محیط نیمه جامد (ژل ) بعنوان فاز ثابت استفاده میشود. این نوع الکتروفورز برحسب نوع ژل به کار گرفته شده به دو نوع الکتروفورز ژل پلی اکریل آمید ( PAGE) و الکتروفورز ژل آگارز تقسیم می شود. الکتروفورز PAGE دارای قدرت تفکیک بسیار بالائی بوده و برای تفکیک پروتئین ها و اسید های نوکلئیک به کار گرفته می شود
۳)الکتروفورز در میدان الکتریکی ضربان دار: چنانچه اشاره شد، هر چه غلظت ژل کمتر باشد با آن می توان مولکولهای بزرگتری را بوسیلة الکتروفورز ، تفکیک کرد. ولی در این رقت محدودیت وجود دارد به طوریکه حتی با رقیقترین ژلهای آگاروز هم نمی توان مولکولهای DNA بزرگتر از 100 کیلو جفت باز را تفکیک کرد.[11]
الکتروفورز در میدان الکتریکی ضربان دار
- الکتروفورز درمیدان الکتریکی ضربان دار تک جهتی(UPFGE )
- الکتروفورز در میدان الکتریکی معکوس (FIGE)
- ژل اکتروفورز در میدان الکتریکی ضربان دار (PFGE)
انواع ژل
آگارز مخلوطي از دو پليساكاريد آگارز و آگاروپكتين است كه از بعضي از انواع گونههاي جلبك دريايي بدست ميآيد
- جداسازي پروتئين هاي بسيار بزرگ
پليمريزاسيون مونومرهاي اكريل آميد و بيس آكريل آميد
- جداسازي پروتئين ها و پلي نوكلئوتيدهاي با طول 5 تا 2000 جفت باز
پلي اكريلاميد نسبت به ژل هاي آگار كندتر صورت مي گيرد. چون اكسيژن آزاد از فرآيند پليمريزه شدن ممانعت به عمل مي آورد.
ژل هاي پلي اكريلاميد طيف كوچكي از جداسازي البته با قدرت تجزيه بالا را دارا مي باشند.
ژل هاي آگار طيف بزرگي از جداسازي را البته با قدرت تجزيه نسبتا پايين دارا مي باشند . [12]
ضخامت ژل
اختلاف در دما بين سطح و عمق سبب ميشود پروتئين در عمق سريعتر از سطح حرکت کند
با افزايش حرارت، حرکت مولکول ها بيشتر شده و پخش خود به خودي نيز رخ مي دهد .
فاكتورهاي مهم
- ميزان بار الكتريكي نمونه
- وزن نمونه
- اندازه و شكل نمونه
- ميزان ولتاژ و جريان اعمالي
- نوع ژل و ميزان تخلخل آن
- نحوه آماده سازي نمونه
- نحوه رنگ اميزي
- عوامل محيطي
آماده سازي نمونه
اولين قدم ليز سلولها و خارج ساختن محتواي پروتئيني آنهاست
روشهاي متفاوت مکانيکي و شيميايي درليز و متلاشي ساختن سلولها به کار گرفته مي شود:
- خارج ساختن موادي نظير نمك ها، ليپيدها، پلي ساكاريدها، و اسيدهاي نوكلئيك.
- افزودن بافرهاي محلول سازي و کائوتروپيک, دترجنت, معرف احيا کننده, و آمفولايت ها.
پروتئينهاي نمونه بايد درحين روند الكتروفورز دوبعدي محلول باقي بمانند [12]
شروع الکتروفورز
- مجموعه ژل و قالب آماده شده را در دستگاه الکتروفورز نصب مي کنيم.
- نمونه قبلا آماده شده به هر چاهک منتقل مي شود.
- مارکرهاي وزن نيز معمولا در چاهک هاي طرفين ريخته ميشود
- حوضک ها از بافر کاملا پر ميشود بعد به جريان برق دستگاه وصل مي شود .
پس از تفکیک, رنگ آمیزی صورت می گیرد !
رنگ آمیزی
- جداسازی ژل بالایی
- قرار دادن ژل در محلول تثبیت کننده
- قرار دادن ژل در محلول رنگ
- انواع مختلف رنگ آمیزی
- رنگ آميزي با رنگهاي آنيونيك نظير آبی كوماسي
- رنگ آميزي منفي با كاتيونهاي فلزي مثل رنگ آميزي زينك يا روي
- رنگ آميزي Silver يا نقره
عوامل محیطی
- اثر حرارت
- اثر سيستم هاي بافري و pH
- منبع الکتريکي
بهترين روش آناليز با استفاده از کامپيوتر صورت مي پذيرد
- تشخیص نقاط کمرنگ
- مقایسه تصاوير ژل هاي متفاوت
- ويراستن تصاوير
- نرماليزه کردن تصاوير [12]
الكترودياليز
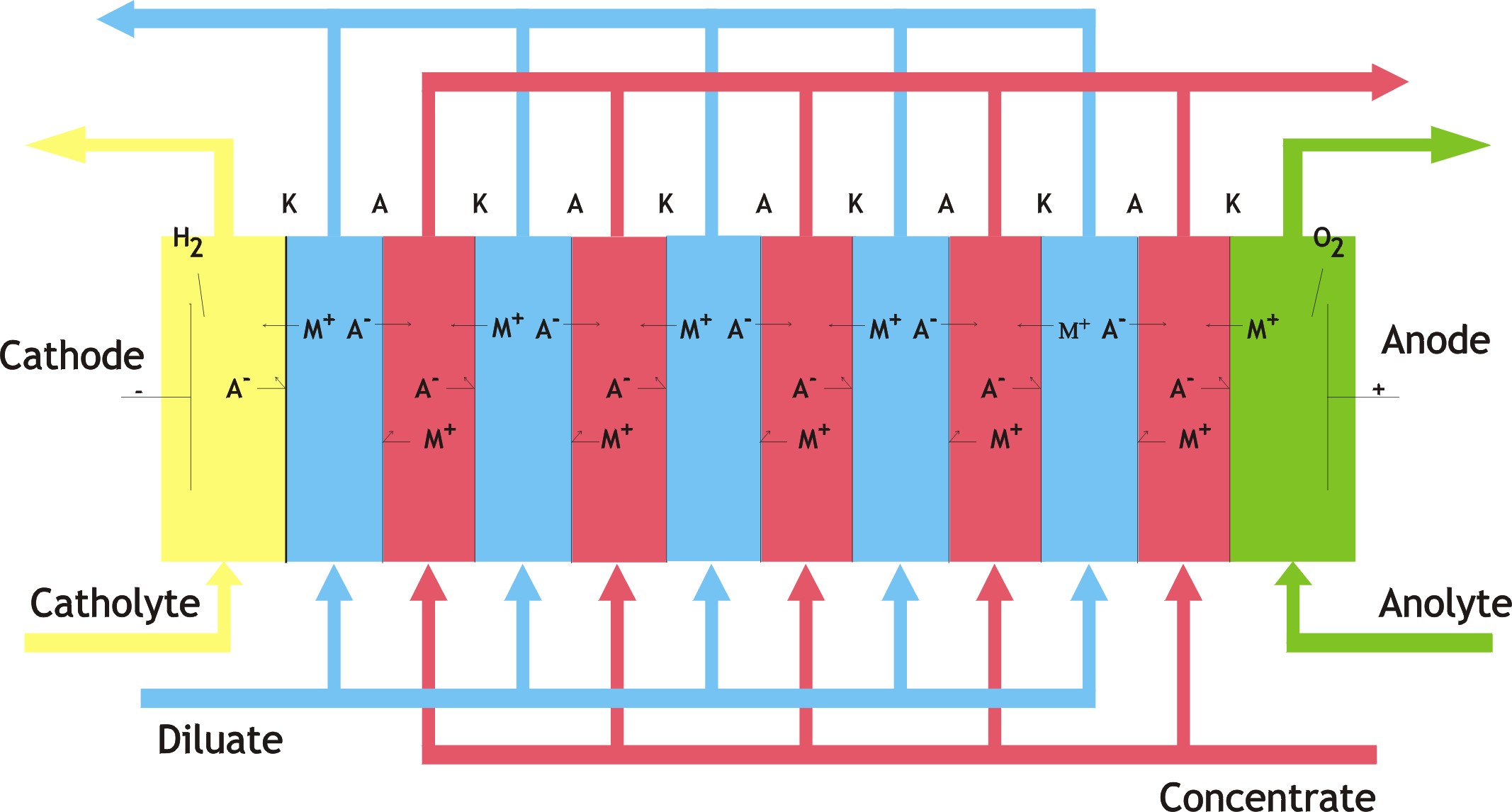
الکترو دیالیز (Electrodialysis)
الکترو دیالیز با علامت مخفف ED نشان داده می شود. یک فرایند جداسازی غشایی می باشد که درآن از اختلاف پتانسیل الکتریکی به عنوان نیروی محرکه جهت انتقال یون ها استفاده می شود . در این سیستم از غشاهای پلیمری حاوی رزین های تبادل یونی استفاده می گردد. این رزین ها بر روی پارچه هایی پلیمری مانند پلی اتیلن پوشش داده شده اند . پرده های کاتیونی نسبت به کاتیون ها تراوا می باشند و آنیون ها فقط می توانند از غشاهای آنیونی عبور نمایند.[8]
فضای بین دو غشای غیر همنام سل نامیده می شود . در سیستم های پیشرفته دستگاه الکترودیالیز به شیوه ای طراحی و بهره برداری می گردد که در حدود هر 15 دقیقه یک مرتبه قطب کاتد و آند جابجا می شوند و به طور اتوماتیک از رسوب روی الکترودها و گرفتگی غشاها کاسته می شود .غشاها توسط جدا کننده های پلیمری از یکدیگر مجزا می شوند به طور معمول ضخامت این توری ها در فضای بین غشاء ها نیم میلی متر و در کنار الکترودها یک میلی متر می باشد.
نکات مهم در طراحی و بهره برداری از سیستم های الکترودیالیز
- کیفیت آب ورودی بیشترین اهمیت را در ثابت نگه داشتن مشخصات آب خروجی دارد . یون های مهم در تصفیه آب شامل سدیم ، کلسیم ، منیزیم ، آهن ، سیلیس ، کلرید و بی کربنات می باشند. هر چند تغییر در مشخصات آب ورودی موجب تغییر در کیفیت آب خروجی می گردد.
2) دمای آب ورودی اثر فوق العاده مهمی بر روی بازده دستگاه و کیفیت محصول دارد. به طور معمول دمای آب نباید از 10 درجه سانتی گراد کمتر و از 45 درجه سانتی گراد بیشتر باشد.
3) حد مجاز آهن در آب وروی به طور معمول حدود ppm 0/2 می باشد زیرا بیشتر از این مقدار موجب اشکال در فرایند می گردد. یکی از اثرهای منفی یون های آهن و یا آهن معلق ، افزایش مقاومت الکتریکی غشاها می باشد که در اثر رسوب بر روی غشاها یک لایه نارنجی رنگ بوجود می آورند و موجب کاهش کیفیت تولید آب و تغییر در ولتاژ و آمپر مورد استفاده می شود. [9]
4) وجود کلرین در آب ورودی موجب آسیب دیدگی سیستم می شود لذا نباید سیستم راه اندازی شود.
5) وجود هیدروژن سولفاید در آب ورودی مانند حالت بالا موجب آسیب رسیدن به غشا میشود و لذا نباید سیستم راه اندازی شود.
6) حد مجاز آهن و منگنز بر روی هم درآب ورودی ppm 2/0 می باشد.
7) به طور اساسی یکی از عوامل وجود آهن در لوله های انتقال و مخازن سرچاهی خوردگی می باشد و یکی از رایج ترین عوامل خوردگی در آب های زیر زمینی باکتری های احیا کننده سولفات (SRB) می باشد که می توانند به دلیل بی هوازی بودن در چاههای آب وجود داشته باشند و همچنین با استفاده از اکسیژن می توان سولفات موجود درآب را احیا و تولید H2S نمود که در نهایت سولفیت آهن تولید می گردد. بهترین شیوه مبارزه تزریق کلر در سر چاه به میزان باقی مانده در حدود ppm 1 می باشد ولی چون کلرین آزاد برای سیستم زیان بخش است ، باید آب را قبل از ورود به سیستم توسط کربن فعال و یا هر شیوه دیگر کلرین زدایی گردد.
8) در سیستم های الکترو دیالیز اتوماتیک ، هر پانزده دقیقه یک مرتبه پلاریته الکتریکی و مسیرهای الکتریکی تعویض می شوند و این عمل با تعویض قطب کاتد و آند انجام میگیرد که هیچ یک از قطب ها با آب نمک غلیظ برای مدت بیش از پانزده دقیقه در تماس نباشند و نمک انباشته شده را به سرعت حل می نمایند و از سیستم خارج می سازند.
9) محیط آند همیشه در اثر تجمع H+ اسیدی می باشد ، لذا مناسب است که آب در اطراف قطب آند ، حالت سکون داشته باشد تا رسوباتی که در این قطب به وجود آمده است حل و در زمان تخلیه خارج شوند و یا به عبارت دیگر عمل شست و شوی اسیدی در قطب آند انجام شود. به دلیل تعویض قطب ها در هر پانزده دقیقه یک مرتبه این روش کمک فراوانی به تمیز شدن الکترودها می نماید.
10) به طور معمول حداقل فشار سیستم الکترودیالیز atm 15/0 و حداکثر atm 5/1 طراحی می شود.
11) دستگاه نشان دهنده اختلاف فشار بین آب رقیق و غلیظ در ورودی و خروجی مجموعه غشاها به شیوه ای است که اختلاف فشار آب تصفیه شده و آب نمک را نشان می دهد زیرا همیشه باید فشار آب تصفیه در حدود نیم الی یک و نیم اتمسفر بیشتر از فشار آب نمک باشد.
12) جهت کنترل کیفیت آب تولیدی دستگاه اندازه گیری هدایت الکتریکی در قسمت خروجی آب تصفیه شده نصب می شود.
13) در صورت توقف بیش از سی دقیقه در سیستم های الکترودیالیز که به شیوه های دستی یا اتوماتیک عمل می نمایند لازم است در حدود چهار الی هشت دقیقه آبکشی شوند تا نمک های باقی مانده تخلیه شوند و از ایجاد رسوب بر روی غشاها جلوگیری گردد.
14) در صورت افزایش T.D.S آب و کاهش آمپر مصرفی لازم است موارد زیر مورد بررسی قرار گیرند : الف) دمای آب : کاهش یک درجه فارنهایت از دمای آب باعث کاهش یک درصد از آمپر مصرفی می شود ب) کثیف بودن غشاها ج) پوشش سطح الکترودها د) پارگی و یا سوختگی غشاها.
15) در صورت کاهش میزان آب تولیدی ، موارد زیر باید بررسی شود : الف ) گرفتگی صافی ها ، ب ) وضعیت سایر تجهیزات مانند شیرها و پمپ ها ، ج) اختلاف فشار جریان های ورودی و خروجی[9]
16) هرگاه جریان مصرفی بین الکترود کاهش یابد باید بررسی زیر انجام گیرد
الف) اطمینان از بسته نبودن لوله های آب تغذیه الکترودها یا لوله های خروجی الکترودها
ب) اطمینان از برابر بودن فشار ورودی آب الکترودها و فشار ورودی مجموعه غشاها
ج) اطمینان از عدم رسوب روی غشاها ، صفحه های جدا کننده و الکترودها. [10]
کریستالیزاسیون

کریستالیزاسیون متداول ترین فرآیند خالص سازی نهایی بشمار می رود.
تعریف : کریستالیزاسیون به فرآیند تولید ذرات کریستالیاز یک فاز یکنواخت گفته می شود این فاز در فرآیند های بیوشیمیایی معمولا محلول است .
این فرآیند بسیار شبیه فرآیند رسوب دهی است با این تفاوت که ذرات حاصل از فرایند کریستالیزاسیون دارای استحکام و مرفولوژی قویتری نسبت به ذرات تولید شده توسط فرایند رسوب دهی هستند و همچنین شدت هسته زایی درفرآیند رسوب دهی بالاتر است .
کریستالیزاسیون دارای قابلیت تولید فرآورده های بیولوژیک با درصد خلوص بسیار بالا می باشد ( حدود 99/9% ) به همین دلیل در صنعت دار و سازی که نیاز به خلوص بالایی داریم کاربرد فراوانی دارد.
اصول کریستالیزاسیون
ساختار کریستال ها:
کریستال ها به فرم چند وجهی و یا جامد با سطوح تخت تولید می شوند. اگر کریستال ها بصورت سریع در یک جهت رشد کنند شکل سوزنی خواهند گرفت یا ممکن است شش وجهی باشند.
اولین مرحله در فرآیند کریستالیزاسیون هسته زایی است که شامل هسته زایی اولیه وهسته زایی ثانویه است.
هسته زایی اولیه در غیاب کریستال اتفاق می افتد در حالی که هسته زایی ثانویه متأثر از وجود کریستال در محیط است.
هسته زایی اولیه به دو فرم یکنواخت وغیر یکنواخت صورت می گیرد درحالت یکنواخت هیچ ذره خارجی نباید حضور داشته باشد ولی کریستالیزاسیون غیر یکنواخت ذرات اولیه حضور دارند.
در مورد هسته زایی ثانویه می توان گفت که آزمایشات نشان می دهد که به دو صورت هسته زایی تنش و هسته زایی تماس اتفاق می افتد.
هسته زایی تنش بر اثر پدیده تنش در سیال در رشد کریستال ها و هسته زایی تماس بر اثر تجمع کریستال ها با هم و بر اثر سطوح همزن وسط و داخل مخزن اتفاق می افتد.
رشد کریستال :
رشد کریستال بعد از فرآیند هسته زایی اتفاق می افتد که در آن مولکول ها به سطوح کریستال های تشکیل شده اضافه می شوند، به خاطر داشته باشید که شدت رشد مستقل از اندازه کریستال است که این مسئله به عنوان قانون دلتا-ال شناخته شده است. (دربعضی از موارد برای کریستال های خیلی بزرگ صادق نیست)
فرایند رشد کریستالیک فرایند دو مرحله ای است در مرحله اول مولکول های حل شونده به سطح کریستال می رسند و در کریستال مولکول ها باید به کریستال اضافه شوند .
مکانیزم انتقال
- انتقال مولکول ها به سطح کریستال
- جذب سطحی بر روی سطح کریستال
- نفوذ دو بعدی و یک بعدی
از کریستال کننده های ناپیوسته بطور گسترده در صنایع دارویی برای تولید فرآورده های بیولوژیک همچون آنتی بیوتیک ها استفاده می شود.
ازمهمترین ویژگی های سیتم های پیوسته به حداقل رساندن زمان فرآیند و همچنین با وجود اینکه هزینه اولیه درسیستم های پیوسته زیاد است اما دردرازمدت هزینه های عملیات رابه حداقل می رساند.
ازمهمترین مزایای کریستال کننده های بچ بسیارانعطاف پذیرهستند وسرمایه گذاری اولیه آنها نسبت به کریستال کننده های پیوسته بسیارکمتراست.
دراغلب سیستم های بچ برای رسیدن به حالت خالص فوق اشباعیت ازروش رقیق سازی استفاده می کنند درمواردی که نمک استفاده می شود به آن روش نمک زدایی می گویند .اضافه کردن یک کاهنده حلالیت حلشونده برای شروع کریستاله شدن حلشونده مطلوب است.
برای مثال آنتی بیوتیک ها با اضافه کردن یک حلال آبی همچون اتانول درمحلول های آبی کریستاله می شوند.
طراحی وافزایش مقیاس کریستالیزاتورها
از جمله مشکلاتی که در فرآیند کریستالیزاسیون امکان دارد رخ دهد توزیع اندازه ذرات کریستالی خارج ازدامنه مورد نظر است که باعث افت شدت فیلتراسیون کریستال ها درمقیاس بالا می شود. برای حل این مشکل باید شدت هسته زایی وشدت رشد کریستال ها تغییر کند که این کار توسط تنظیم درجه فوق اشباعیت قابل کنترل است . بطور کلی با افزایش درجه فوق اشباعیت شدت هسته زایی بیشتر از شدت رشد افزایش می یابد.
مشکل بعدی درفرآیند کریستالیزاسیون تولید کریستال ها با درصد خلوص پایین تر ازمقدار مورد نظر است . این مشکل بنا به دلایل زیر اتفاق می افتد.
- ته نشینی ناخالصی های موجود در محیط درسطح کریستال
- گیر افتادن ناخالصی ها در فضاهای خالی موجود دربین کریستال مجزای مجتمع شده
- رشد کریستال های ناخالص مجزا بواسطه وجود ناخالصی در محیط
- جانشینی مولکول های ناخالصی به جای مولکول های اصلی در شبکه کریستالی طی فرآیند کریستالیزاسیون
برای حل مشکل وجود ناخالصی در سطح کریستال ها می توان با بهبود روش های جدا سازی جامد-مایع و یا شستشوی سطوح کریستال ها بعد از جداسازی تا حدود زیادی رفع شود .
برای حل مشکل ناخالصی های موجود بین فضا های خالی کریستال های به هم چسبیده با تغییرات شرایط کریستالیزاسیون همچون استفاده از حلال دیگر کاهش می یابد .
با کاهش درجه فوق اشباعیت شدت رشد و شدت هسته زایی کاهش می یابد که این امر باعث به حداقل رسیدن کریستال های مجزای حاصل از ناخالصی ها می شود.
رفع مشکل جانشینی مولکول های خالص به جای مولکول های اصلی طی فرآیند کریستالیزاسیون خیلی مشکل است و در اکثر موارد نیاز به کریستالیزاسیون مجدد داریم.
دوباره کریستاله کردن که به طور وسیع استفاده می شود با انحلال مجدد کریستال ها و اجرای مجدد فرآیند صورت می گیرد.
خشك كردن
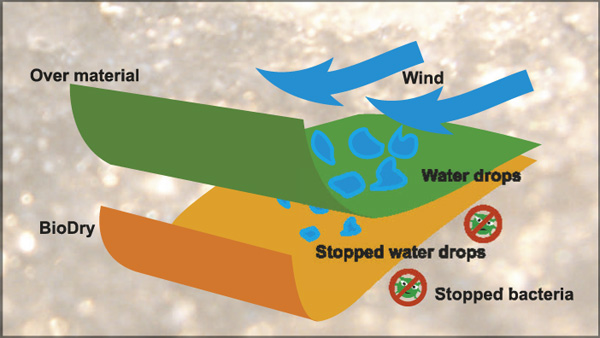
خشك كردن معمولا آخرين مرحله جداسازي يك محصول بيولوژيك است كه از طريق حرارت مواد فرار (آب) را حذف ميكند تا يك ماده جامد به دست آيد .
دلايل خشك كردن يك محصول بيولوژيك :
- نسبت به تخريب شيميايي و فيزيكي در طي ذخيره سازي در فرمولاسيون مايع حساس مي باشد .
- راحتي مصرف آن به صورت جامد
- حذف مواد نامحلول ضروري
- اقتصادي بودن ذخيره كردن آنها به صورت جامد
اصول خشك كردن :
- آب در جامدات بيولوژيك و گازها
آزاد
جذب شده
- انتقال حرارت
هدايت ( از سطح تماس گرم ماده )
جابجايي ( از طريق گازي كه در تماس با ماده خشك شونده است )
- انتقال جرم :
درخشك كردنهاي جابجايي فرايند خشك كردن توسط انتقال جرم محدود ميشود . خشك كردن جابجايي ، ابتدا رطوبت جامدات مرطوب تبخير شده و سپس وارد فاز گازي ميشود كه از روي سطح اين جامدات عبور ميكند . بعد از يك دوره كوتاه گرم شدن اوليه ، سرعهت حركت آب به سطح به حد كافي است كه سطح اشباع از بخار قرار گيرد ، و بالطبع سرعت خشك كردن براي يك دوره زماني كه دوره سرعت ثابت خشك كردن ناميده مي شود ثابت باقي مي ماند.
توصيف و عمليات خشك كن ها : چندين نوع خشك كن براي خشك كردن جامدات بيولوژيك استفاده ميشود :
- خشك كن هاي قفسه اي تحت خلاء
- خشك كن هاي غير مداوم دوار تحت خلاء
- خشك كن هاي انجمادي
- خشك كن هاي پاششي
- خشك كن سيني دار تحت خلاء : در خشك كن سيني دار تحت خلاء سيني ها با محصول مورد نظر پر شده و داخل قفسه هايي كه جهت تبادل گرمايي سيستم چرخش آب گرم در آنها تعببيه شده قرار داده ميشوند . براي محفظه حاوي سيني ها از خلاء استفاده ميشود تا فرايند خشك كردن را تسريع كند و امكان خشك كردن را در دماي پايين تر فراهم نمايد . اين نوع خشك كردن به طور گسترده براي فراورده هاي دارويي مثل آنتي بيوتيك ها ، كه اغلب شكل كريستال داشته و حساسيت زيادي نسبت به گرماي زيادي دارند استفاده مي شود .
- خشك كن هاي دوار ناپيوسته تحت خلاء : در خشك كن هاي دوار ناپيوسته تحت خلاء گرما توسط آب گرم و ديگر محيطهاي تبادل گرمايي كه از ميان يك ژاكت استوانه دوار دوجداره عبور ميكند فراهم ميشود . در اين خشك كن جامدات به طور پيوسته با چرخش استوانه معلق ميشوند تا ذرات جامد در تماس با ديواره هاي استوانه و يا تماس با يكديگر قرار گيرند . اين نوع خشك كن ها براي خشك كردن فراورده هاي بيولوژيك كه ميتوانند توسط خشك كن سيني دار تحت خلائ خشك شوند به كار ميرود ، اما وقتي كه ذرات مواد جامد مرطوب در اثر حركت معلق تشكيل ذرات و توده هاي بزرگتر را ميدهند و يا وقتي كه به سطح فلزي استوانه ميچسبند نمي توانند استفاده شوند .
- خشك كن هاي انجمادي ( فريز داير ) : در خشك كردن انجمادي لازم است دما و فشار هر دو در طي فرايند خشك كردن كنترل شوند . محصول خشك شونده ميتواند به صورت ويال و يا داخل سيني ها باشد . خشك كن انجمادي دارويي ميتواند يك فراورده مايع را داخل ويال ها خشك كند وقتي ويال ها داخل سيني قرار داده ميشوند درب ويال به صورت جزئي بسته ميشوند تا بخار آب بتواند از آن خارج شود . پيستون هيدروديناميك اين امكان را فراهم ميكند تا درب ويال ها در پايان خشك كردن به طور كامل بسته شود يك سيال ناقل حرارت در ميان سيني ها قرار داده ميشود تا دماي ويال ها را كنترل كند .
آب آزاد در مرحله اول خشك كردن حذف ميشود دماي بيشتر سيني و زمان اضافي براي حذف آب پيوندي در مرحله دوم خشك كردن لازم است . نمدارهاي دما و فشار به عنوان تابع زمان در مراحل مختلف انجماد ، خشك كردن اوليه و خشك كردن ثانويه در شكل نشان داده شده است . زمان لازم براي تكميل دوره خشك كردن معمولا 24 تا 48 ساعت طول ميكشد . در طي فرايند خشك كردن انجمادي مهم است كه دماي محصول در حدي نباشد كه باعث بهم خوردن ساختار كريستالي و بالطبع كاهش فعاليت آن شود .
خشك كردن انجمادي معمولا تنها براي فراورده هاي بيولوژيكي كه حساسيت بالا به گرما دارند استفاده ميشود . بيشتر پروتئينها در اين گروه از فراورده ها قرار ميگيرند چون بعد از خشك كردن اوليه فاز مايع در محول وجود ندارد واكنش هايي مانند هيدروليز ، اكسيداسيون ، بازارايي از پيوند ديسولفيدي و ... اساسا حذف خواهند شد . مزيت ديگر خشك كردن انجمادي اين است كه محصول سطح مقطع ويژه خيلي بزرگي دارد كه منجر به حل شدن سريع و كامل آن ميشود .
- خشك كن هاي پاششي : خشك كن پاششي يك خوراك مايع مانند را با پاشيدن به داخل گاز گرم ، معمولا هوا ، به ذرات خشك تبديل ميكند . عمده خشك كن هاي پاششي كه در مقياس هاي تجاري به كار ميروند از جريان همسوي گاز و خوراك استفاده مي كنند . سه واحد فرايندي پايه : ريز شدن مايع ، اختلاط گاز با قطرات مايع و خشك كردن قطرات مايع ، در خشك كردن پاششي درگير هستند . اين ذرات خشك مي توانند توخالي يا پر در اندازه 2 تا بيش از 500باشند .
كاربرد خشك كنهاي پاششي براي خشك كردن بيشتر فراورده هاي حساس به گرما شامل شير ، قهوه ، خون ، اسپورها و ميكروارگانيسم هاي مختلف و آنتي بيوتيك شده است .
افزايش مقياس و طراحي سيستم هاي خشك كردن : امكان طراحي دقيق و مطمئن خشك كن صنعتي براي خشك كردن فراورده هاي بيولوژيك تنها بر اساس خواص فيزيكي مواد هنوز فراهم نشده است . روابط تعميم يافته تئوري و تجربي براي تخمين اندازه خشك و زمان خشك كردن و همچنين آناليز عملكرد خشك كن و پيش بيني اثرات تغييرات شرايط عملياتي توسعه داده شده اند .
- افزايش مقياس خشك كن هاي سيني دار تحت خلاء : افزايش مقياس اين خشك كن ها نسبتا ساده است يك روش مناسب براي سنجش خشك كردن در مقياس آزمايشگاهي و نيمه صنعتي استفاده از همان عمق موادي است كه قرار است در مقياس صنعتي استفاده شود . اثر تغيير شرايط روي افزايش مقياس مي تواند با استفاده از رابطه تعيين زمان خشك كردن هدايتي محاسبه شود : بازده حرارتي خشك كن هاي سيني دار تحت خلاء بين 60 تا 80 درصد است .
- افزايش مقياس خشك كن هاي دوار ناپيوسته تحت خلاء : با افزايش مقياس يك خشك كن ناپيوسته دوار تحت خلاء مي توان دريافت كه سطح مقطع گرم شده در واحد حجم داخلي ثابت نميماند . براي مثال اگر فرض كنيم كه يك خشك كن يك مخروط دو جداره كامل ، وقتي حجم در اثر افزايش مقياس حدود 10 برابر افزايش مقياس داده ميشود سطح گرم شده حدود 6/4 برابر افزايش مي يابد .
- افزايش مقياس خشك كن هاي انجمادي : دو شرط اساسي در توسعه اين كار تعيين فرمولاسيون محصول نهايي و تعيين شرايط براي چرخه خشك كردن انجمادي مي باشد براي فرمولاسيون محصول نهايي جهت حفظ فعاليت مواد مختلفي مثل بافرها جهت كنترل PH اصلاح كننده كشت نمكي سيستم براي تنظيم فشار اسمزي اصلاح كننده ساختار مواد ، تثبيت كننده يا محافظت كننده مواد فعال و بازدارنده فراريت مواد اضافه مي شود . مواد افزودني عموما شامل : مانيتول ، گلايسين ، لاكتوزط ، سوكروز و دكستران هستند . سه سيكل عمده در فرايند خشك كردن انجمادي ، انجماد ، خشك كردن اوليه و خشك كردن ثانويه هستند . از اين رو معمولا سه مرحله آناليز براي تعيين شرايط طراحي خشك كردن انجمادي به كار مي رود .
- افزايش مقياس خشك كن هاي پاششي : براي افزايش مقياس و طراحي خشك كن هاي پاششي صنعتي لازم است برسي ها و تجزيه و تحليل ها در مقياس هاي پايين تر براي شرايط خشك كني جهت توليد ذرات غير چسبنده بزرگتر و با رطوبت مطلوب انجام شود . براي مواد بيولوژيك ، لازم است درجه خشكي و شرايط عملياتي كه محصول فعال و پايدار را تحويل مي دهد تعيين شود . در افزايش مقياس خشك كن هاي پاششي ، متغير كليدي زمان ماند هوا در محفظه خشك كن است زمان ماند با تقسيم حجم محفظه به سرعت جريان حجمي محاسبه مي شود .
خشک کن ها

در بین کلیه عملیات واحدهای صنعتی در مهندسی شیمی ، شاید عملیات مربوط به خشک کردن مواد ، بیشترین کاربرد را داشته باشد. به این جهت ، مکانیسم خشک کردن و طراحی دستگاههای مربوطه در مقیاس صنعتی از اهمیت ویژه ای برخوردار است. در اکثر عملیات مربوط به تولید مواد ، مخصوصا در صنایع شیمیایی ، یک یا چند مرحله عملیات خشک کردن در یکی از اشکال متنوع آن وجود دارد. عملیات خشک کردن بر حسب موادی که باید خشک شوند، ممکن است از چند ثانیه تا چندین روز طول کشد
خشک کن های سینی دار تحت خلا
این دستگاه ها نیز مشابه خشک کن های سینی دار مستقیم ساخته می شوند با این تفاوت که از درب های درزگیری شده استفاده می شود تا بتواند خلاء ایجاد شده در خشک کن را نگهدارد. دراین خشک کن هوا یا گاز دیگری جریان نمی یابد. سینی های محتوی جامد روی قفسه هایی قرار می گیرند که توسط آب داغ یا بخار گرم می شوند و حرارت به طریق هدایت به جامد منتقل می گردد. بعد از بارگذاری و آب بندی ، هوای موجود در خشک کن توسط پمپ های خلاء یا اجکتور مکیده شده و بخار خروجی کندانس می شود. در نوع دیگری )Agitated Pan Dryer) از این خشک کن ها برای خشک کردن خمیرها و لجن ها از ظروف استوانه ای به قطر 1تا2متر و ارتفاع 30تا60 سانتیمتر که مجهز به همزن می باشند استفاده می شود که داخل کابین خلاء قرار می گیرند. این ظروف توسط ژاکت های حرارتی با آب داغ یا بخار گرم می شوند.
این خشک کن هاعمدتا" پرهزینه هستند و تنها در مواردی که می بایست ماده در دمای پایین و در غیاب هواخشک شود استفاده می گردد. از جمله می توان به مواد دارویی اشاره کرد.
در این نوع از سیستم های خشک کن، برای قرار دادن محصول در معرض هوای گرم در یک فضای بسته ، از سینی یا وسایل مشابه نگه دارنده استفاده می شود، سینی های حاوی محصول در داخل یک کابینت یا محیط مشابه و در معرض هوای گرم قرار داده می شوند تا فرآیند خشک شدن انجام شود . حرکت هوا بر سطح محصول با سرعت نسبتا زیادی صورت می گیرد ، تا اطمینان حاصل شود که انتقال جرم و حرارت با بازده ای بالایی انجام می شود با یک تغییر جزئی در خشک کن کابینتی می توان در داخل محفظه آن خلاء ایجاد کرد. در این نوع سیستم خشک کن، با استفاده از خلاء ، فشار بخار در فضای اطراف محصول در حداقل ممکن نگه داشته می شود. کاهش فشار همچنین باعث کاهش دمای تبخیر رطوبت محصول نیز می شود که در نتیجه موجب بهبود کیفیت آن خواهد شد.
در بیشتر حالات خشک کن های کابینتی به صورت ناپیوسته کار می کنند واز معایب آن ها خشک شدن غیر یکنواخت محصول درون سیستم می باشد. معمولا برای بهبود یکنواختی بیشتر باید سینی های حاوی محصول جابه جا شوند.
خشک کن های دوار نا پیوسته تحت خلاء
دستگاه خشک کن دوار برای خشک نمودن موادی مانند سنگ آهک، خاکستر، خاک رس و ... مورد استفاده قرار می گیرد. این دستگاه در صنایع تهیه مصالح ساختمانی، متالورژی، صنایع شیمیایی، و صنعت سیمان بهکار میرود. از جمله مزایای این نوع ” خشکن کن " ساختار مستحکم، ظرفیت بالا، مصرف انرژی پایین و نگهداری و سرویس آسان آن می باشد.
« طراحی خشك کن دوار»
برای طراحی یک خشکگن دوار باید موارد زیر را محاسبه کرد:
1) طول و قطر خشککن
2) شیب خشککن
3) مقدار هوای لازم برای عمل خشککردن
4) مقدار حرارت لازم
5) جهت جریان
6) تعداد دور استوانه در واحد زمان
برای بدست آوردن موارد بالا بایستی یک سری معلومات داشته باشیم که عبارتنداز:
1) رطوبت و دمای هوای موجود
2) رطوبت و دمای هوای خروجی از گرمکن
3) رطوبت و دمای هوای خروجی از خشککن
4) رطوبت ماده ورودی
5) مقدار محصول در واحد زمان
6) میزان رطوبت محصول
اصول کارکرد:
دستگاه خشککن از یک استوانه افقی دوّار تشکیل شده است. مواد از یک سمت دستگاه وارد استوانه شده و از سمت دیگر خارج می گردد. در خشک کن نوع مستقیم، گازهای گرم از میان استوانه می گذرند و در تماس مستقیم با مواد می باشند. حرکت گازهای گرم می تواند همسو یا مخالف جهت جریان مواد باشد. استوانه دارای یک سری پره می باشد که مواد را برداشته و با رها سازی مواد، عبور مواد به صورت بارشی از میان جریان گاز گرم را ممکن میسازد.
ویژگی ها و مزایای اصلی:
1- استفاده از دو نوع صفحه بردارنده مواد ایکس و اچ
2- سیستم انتقال قدرت بهبود یافته (استفاده از دنده دارای قابلیت تعویض دندانه، بنابراین تعمیرات و نگهداری آسان)
3-عملکرد خودکار با استفاده از سیستم کنترل مرکزی
خشک کن های انجمادی
در خشک کردن انجمادی ، با کاهش دمای محصول ، قسمت اعظم رطوبت آن به یخ تبدیل شده و سپس با کاهش فشار محیط ، تصعید می گردد. فرآیند خشک کردن انجمادی را می توان برای بسیاری از مواد غذایی به خصوص محصولاتی که کیفیت ۀن ها از نظر مصرف کننده حائز اهمیت است ، به کار برد در طول خشک کردن انجمادی ، فرآیند های انتقال جرم و حرارت به طور مطلوبی انجام می شوند. بسته به شکل سیستم خشک کن ، انتقال حرارت ، از طریق لایه منجمد یا لایه خشک محصول صورت می گیرد . بدیهی است، انتقال حرارت از طریق لایه منجمد ، سریع بوده بنابراین محدود کننده ی سرعت خشک شدن نخواهد بود. سرعت انتقال حرارت از طریق لایه خشک کند است، زیرا ضریب هدایت حرارتی ساختمان های کاملاً متخلخل در شرایط خلاء پایین است. در هر دو حالت ، انتقال جرم در لایه خشک محصول انجام می شود . از آنجایی که سرعت نفوذ مولکولی در خلاء کند است، بنا براین انتظار می رود که سرعت نفوذ بخار آب ، عامل محدود کنندهی سرعت خشک شدن باشد.
مزایای فرآیند خشک کردن انجمادی ، بالا بودن کیفیت محصول تولیدی به دلیل پایین بودن دما در حین تصعید و حفظ ساختمان محصول است . این مزیت ها در برابر مصرف انرژی برای انجماد و ایجاد خلاء متعادل بوده و توجیه کننده فرآیند است.
این روش برای مواد غذایی مایع مثل شیر ، آبمیوه ، آب گوجه فرنگی و آب پنیر به کار می رود در این روش ماده غذایی در دستگاه تبخیر کننده تغلیظ و سپس توسط یک اتو مایزر به صورت پودر به داخل خشک کن پاشیده می شود و از قسمت پایین هوای گرم با ذرات ماده غذایی برخورد نموده و رطوبت را از ماده غذایی جدا می کند . در این سیستم مایعی که قبلا تا حدودی تغلیظ گردیده است تحت اثر فشار به درون محفظه ای که دارای هوای داغ است به صورت ذرات بسیار ریز پاشیده می شود .
اصول کار خشککن پاششی
خوراک از طریق یک مخزن و بهوسیله پمپ، به دستگاه اتمایزر که در بالای محفظه خشککن قراردارد، منتقل میشود و به قطرات ریز مایع تبدیل میگردد. در محفظه خشککن این قطرات در تماس با هوای داغ قرار میگیرند. معمولاً هوا با توجه به نوع محصول، توسط هیتر بخار یا مشعل گرم شده و توسط یک فن به داخل محفظه فرستاده میشود. تبخیر سریع مایع (که اغلب آب میباشد) باعث میشود که خشک شدن به سرعت و طی چند ثانیه انجام گیرد. پودر بعد از خروج از محفظه خشککن توسط سیستمهای جداساز نظیر سیکلون و فیلترکیسهای از هوا جدا میشود. پودر بدست آمده قبل از بستهبندی خنک میشود، این عمل توسط هوای خنک انجام گرفته و تواماً میتوان پودر را توسط این سیستم به قسمتهای دیگر، منتقل نمود. جهت کنترل عملکرد خشککن و تولید محصول مناسب، کنترل پارامترهایی نظیر درجه حرارت هوای ورودی و خروجی، کنترل میزان خوراک و درصد مواد جامد آن ضروری است.
به طور کلی در یک سیستم خشککن پاششی چهار مرحله زیر به ترتیب صورت میگیرد:
الف) اسپریکردن خوراک
ب ) تماس بین فاز هوای داغ و مایع اسپری شده
ج) خشک شدن قطرات اسپری شده
د) جدا سازی محصول خشک شده از هوا
این سیستم عموماً شامل اجزاء اصلی زیر میباشد و در موارد بخصوص، تجهیزات جانبی دیگری نیز در کنار آن قرار میگیرند.
- محفظه خشککن
- فنهای هوا
- سیستم تولید هوای گرم
- توزیع کننده هوا
- سیستم خوراک دهی
- سیستم اسپری کننده
- سیستم جداسازی پودر
- سیستم انتقال و خنک کردن پودر
- سیستم کنترل و ابزار دقیق
فرآیند خشک کن های انجمادی
این فرآیند برای مواردی به کار می رود که بسیار حساس به حرارت هستند بدون این که تخریب شدید رخ دهد در پروتئین ها، محصولات خونی و میکروارگانیسم ها در این فرآیند حلال ما که معمولا آب است تصعید تحت خلاء از مرحله فاز جامد به مرحله فاز گازی مستقل می شود
مراحل خشک کردن به روش انجمادی را توضیح دهید؟
مرحله اول:انجماد سازی :در این مرحله مهم است مواد را زیر نقطه سه گانه خشک کنیم نقطه سه گانه پایین ترین دمایی است که در آن فاز های جامد و مایع می توانند همزمان وجود داشته باشند این کار باعث می شود که عمل تصعید رخ دهد-درموارد مواد غذاییویا موادی که از سلول های زنده تهیه شده اند به منظور بردن مواد به نقطه سه گانه و اجتناب از تشکیل کریستال های بزرگ یخ معمولا دماهای انجماد بین 50- تا80- صورت می گیرد
مرحله دوم:به کار گیری خلاءدر این مرحله مواد انجماد شده باید به یک منبع خلاءکافی متصل شوندتا فشار در نقطه سه گانه نگه داشته شود-زیرا در طی خشک کردن فشار بخار پایینی ایجاد شده که منبع خلاءباید فشار بخار تشکیل شده را کاهش دهد تا از افزایش بخار در بالای نقطه سه گانه جلوگیری شود
همچنین خلاءبه صورت تصعید سرعت می بخشد.
مرحله سوم:مرحله تصعید:گرمایی تصعید توسط هدایت وتشعشع تا مین می شود تحت این شرایط یخ به آرامی تعید شده وجامد متخلخلی باقی می گذرد که هنوز5./. رطوبت دارد
مرحله تصعید دارای 2 مرحله است :1)خشک کردن اولیه 2)خشک کردن ثانویه
1)در مرحله خشک کردن اولیه حدود95 درصد آب موجود در مواد تصعید می شود که این مرحله به کندی انجام می شود ومحصول نهایی فقط 5./. رطوبت دارد
2)در مرحله خشک کردن ثانویه مولکول های آب منجمد نشده حذف می شوند.این بخش از فرآیند توسط ایزوترم های جذب سطحی ماده کنترل می شود –در این فاز دما بالا می رود می تواند بالا تر از ......هم باشد این دما می تواندهر نوع برهم کنش شیمیایی و فیزیکی را که بین مولکولها را آب ومولکولهایآب ومولکولهای منجمد شده تشکیل شودرا از بین بببرد معمولا فشار در این مرحله کاهش پیدا می کند تا عمل واجذب راحتر را انجام شود
مرحله پنجم:بسته بندی: باید توجه شود به محصولات خشک شده انجمادی تا از محافظت در برابر رطوبت مطمئن شویم ظروف باید کاملا بسته باشد و بدون تماس با اتمسفر بسته بندی شوند
برای تشکیل تولید کریستال های بزرگ یخ سازی به چه روشی انجام می شود؟
برای تولید کریستال های بزرگتر محصول باید به آرامی منجمد شود ویا دما به صورت چرخشی کم و زیاد شود که این فرآیند چرخشی را annelig یاسرد سازی آهسته می نامند از معایب روش منجمد سازی تشکیل کریستال های بزرگیخ است برای جلوگیری از این روش باید منجمد سازی سریع انجام شود به منظور بردن مواد به زیر نقطه سه گانه و اجتناب از تشکیل کریستال های بزرگ معمولا دماهای انجماد بین 50- تا80- صورت می گیرد
چرا از روش خشک کردن freez drting
1- خرابی حداقل در محصول
2- رطوبت نهایی در محصول بسیار کم است
3- برای نگهداری طولانی مدت محصول
4- سهولت در ترکیب جدید
5- برای ترکیباتی که دوز دقیق دارند(مثل داروها)
چه هنگام از روش های خشک کردن انجمادی استفاده می کنیم ؟
1- برای محصولات ناپایدار 4-محصولاتی که مقدار دوز دقیقی دارند
2- محصولاتی که ارزش بالایی دارند 5-ترکیب مجدد آسان باشد
3- خشک کردن به روش استریل 6- زمان نگهداری طولانی باشد
7-نگه داشتن شکل وفرم محصول مهم باشد
نکات مهم در فرآیند انجمادی:
1- عمل تصعید باید در دماهای زیر صفر رخ دهد
2- عمل تصعید زمانی اتفاق می افتد که فشار زیر نقطه سه گانه باشد
3- این فرایند چون در دماهای پایین اتفاق می افتد گرمای مورد نیاز برای تصعید کم خواهد بود
سرعت خشک کردن به عوامل زیر بستگی دارد
1-ضخامت محصول:هر چه ضخامت کمتر باشد سرعت خشک کردن افزایش می یابد
2- غلظت محصول: محصولات غذایی با درصد قند بالاتر دارای سرعت خشک کردن پایینتری هستند
3- افزایش سطح:هرچه مساحت سطح بیشتر باشد عمل تصعید زود تر انجام می شود
محدودیتهای فرایند خشک کردن :
1- محصولاتی که به روش انجمادی خشک می شوند ........پلاسما ی خون اگر چه از لحاظ تئوری آسان هستند ولی از لحاظ عملی مشکلاتی دارند
2- کاهش نقطه انجماد که به دلیل وجود ماده حل شونده رخ می دهد به این معناست که اگر ناخالصی را به آب اضافه کنیم دمای انجماد10- تا...........کاهش پیدا می کند
3-تصعید تنها در سطح منجمد شده اتفاق می افتد چون این فرایند به آهستگی انجام می گیرد باید سطح مساحت را زیاد کنیم
4- هرچه مساحت سطح زیادتر باشد عمل تصعید زودتر انجام می شود
5- در فشارهای پایین حجم بزرگی از بخارآب تولید می شود که باید حذف شود برای جلوگیری از افزیش فشار در بالای نقطه سه گانه
6- موادی خشک شده به این روش چون رطوبت گیر هستند باید درهنگام بسته بندی از جذب دوباره رطوبت جلوگیری شود
مزایایی روش خشک کردن انجمادی :
1- چون این فرایند در دماهای پایین اتفاق می افتد تخریب شیمیایی به ویژه هیدرولیزبه حداقل می رسد
2-این فرایند به دلیل این تحت خلا اتفاق می افتد در نتیجه تماس کمی با هوا وجود می آید که این عمل اکسیداسیون می رسد
3- محصول فریز شده دارای حجم یکسانی است با ماده اولیه –وبسیار سبک ومتخلخل است
4- ..........متخلخلمحصول آن را برای انحلال راحت تر می کند
5- محصول نهایی دارای بافت چروکیده شده و سفتی نیست
6- قبل از خشک کردن هیچ مرحله تغلیظی وجود ندارد بنابراین نمک ها تغلیظ نمی شوند –پروئتین ها نمی شوند ولی در دیگر روشها این اتفاق می افتد
7- از لحاظ فاکتورهای حسی مثل بو-طعم-رنگ و.همچنین از لحاظ مواد مغزی در محصول نهائی بدون تغییر باقی می ماند
معایب روشfree dring
1- تخلخل وقابلیت حل شدن زیاد وخشک شدن کامل محصول کاملا رطوبت گیر را تولید می کند بنابراین محصولات خشک شده در ظروف نهائی باید تحت شرایط خاصی بسته بندی شوند
2- در این فرایند از دستگاهها و تجهیزات پیچیده ای استفاده می شود که خیلی گران هستند این روشهای معمولی برای خشک کردن نیست فقط برای محصولات پر ارزش استفاده می شود
منابع
1.سید عباس شجاع الساداتی،"کروماتوگرافی مایع با کارایی بالا"،انتشارات دانشگاه تربیت مدرس. صفحه351-458،1371
- مرتضی صادقی (هیات علمی دانشگاه صنعتی اصفهان)-مهندس علیرضا وفائی منش. "مقدمه ای بر غشاء وفرآیندهای غشائی"
- سیدعباس شجاع الساداتی –محمدعلی اسداللهی (دانشگاه تربیت مدرس) "بیوتکنولوژی صنعتی"
- Anspach E.F., Curblo D.C., Hartmann R., Garke G., Deckwea W.D., Expanded-bed chromatography in primary protein purification, Journal of Chromatography, Vol.865,129-144 ,1999.
- Garcia A.A., Bonen M.R., Ramirez-Vick J., Sadaka M., Vuppu A., Chromatography, In Bioseparation process science, Blackwell Science 178-223,1999.
- Dechow F.J., Ion Exchange, In Fermentation and Biochemical Engineering Handbook, Noyes Publications, 2nd ed.,382-472,1997.
- Dorsy. J.G, Cooper W.T., Retentition mechanisms of bonded-phase liquid chromatography, Anal. Chem. Vol. 66,1994.
- سایت بهداشت محیط ایران ، "مقایسه سیستم های الکترودیالیز و اسمز معکوس"
- http://www.environmentalhealth.ir/pages/269/
- http://elm24.com
- "الکترودیالیز در تصفیه آب و فاضلاب"،1391
- "فناوری غشایی و کاربرد آن در جداسازی گاز"،1391
- http://bio1.ir/
♦♦♦ در صورت داشتن هرگونه سوال در مورد این موضوع برای ما نظر بگذارید (در پایین همین صفحه). در اسرع وقت به تمامی سوالات شما توسط کارشناس مربوطه پاسخ داده خواهد شد. با تشکر ♦♦♦
مطالب مشابه :
- سمینار چیست؟|توضیح کامل |بررسی تفاوت همایش، کنفرانس، سمینار، کنگره، فراخوان، گردهمایی، میتینگ، جشنواره، کنوانسیون و کارگاه
- پایاننامه چیست؟| مراحل نوشتن پایان نامه و شرح کامل آن| تخصصی
- آموزش پروپوزال نویسی برای پایان نامه و رساله دکتری | تخصصی | انجام پروپوزال
- بهینهسازی تولید | طراحی آزمایشها با روش متدولوژی سطح پاسخ (RSM)
- رفع اشکال تخصصی روش بلاتینگ نیمه خشک (سمی درای) | بیوتکنولوژی
- آموزش قدم به قدم طراحی ازمایش (RSM) | با نرم افزار دیزاین اکسپرت +نحوه ارائه در مقالات علمی و پایان نامه ها
- رفع اشکال تکنیک وسترن بلات(Western blot)|بصورت کامل و تخصصی | بیوتکنولوژی
- طراحی آزمایش چیست؟ | آموزش کلیات به همراه توضیحات کامل هر مرحله
- آموزش RSM| تحلیل نمودارهای آماری در روش سطح پاسخ | نرم افزار دیزاین اکسپرت