مطالب مرتبط:
- فناوری DNA نوترکیب |بیوتکنولوژی
- تولید پروتئین نوترکیب مزایا و چالش ها
- مهندسی ژنتیک
- کریسپر چیست؟ به زبان ساده | مهندسی ژنتیک | بیوتکنولوژی
- راهنماي اخلاقي پژوهشهاي ژنتيك
- کاربردهای بیوتکنولوژی در صنایع غذایی
GENE CLONING
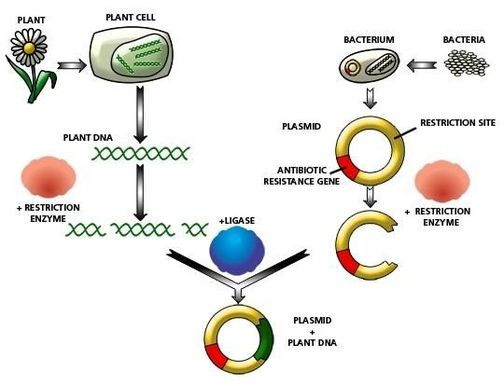
کلونینگ ژن پروسه ای است که طی آن یک DNA خارجی را وارد سلول میزبان انتخابی [1]( hust می کنیم و میزبان را برای سنتز پروتئین مرتبط با آن قطعه ژنی به خدمت میگیریم.
Gene cloning شامل مراحل زیر است :
1 – جدا کردن قطعه ژنی مد نظر از بقیه ژنها
2 – انتخاب وکتور مناسب
3 – اینتگره کردن ژن با وکتور و تشکیل پلاسمید کامل ( DNA Recambinant )
4 – انتقال پلاسمید به hust ( Transformation or Translection )
5 – تکثیر (Replication ) و انتقال پلاسمید حاوی ژن از سلول مادر به سلولهای دختری
6 –رونویسی (Transcription )
7 – ساخت پروتئین در فرایند ترجمه (Translation )
مثال : تولید انسولین توسط Ecoli : انسولین یک پروتئین یوکاریوتی است لذا ژن آنرا از سلول یوکاریوت ( Mamalian call ) جدا کرده و مراحل 1 تا 7 فوق را انجام می دهیم .(host همان Ecoli است که انسولین را می سازد ).
technology Recambinant تکنولوژی نوترکیبی :
منظور تولید موجودی نوترکیب است که به عنوان مثال در شیرش ماده ی دارویی TPAتولید میشود
آیا هر قطعه ژنی را می توان به منظور Transcription (رونویسی ) وارد سلول میزبان کرد ؟
یک قطعه ژنی بی سر و ته (!) یعنی بدون همراه داشتن سیگنال در داخل host خوانده نمی شود, بلکه باید یکسری سیگنالهایی را در قالب پسوند و پیشوند داشته باشد تا توسط سلول میزبان بتواند رونویسی شود .
ویژگی پلاسمیدها :
1 - Indipended of the host cell chromosome خودبخودی و مجزا از کروموزوم اصلی دچار replication (تکثیر ) شوند .
2 – اغلب ژنهای مقاوم به آنتی بیوتیک را به همراه دارند – به عنوان Select marker به کار می رود .
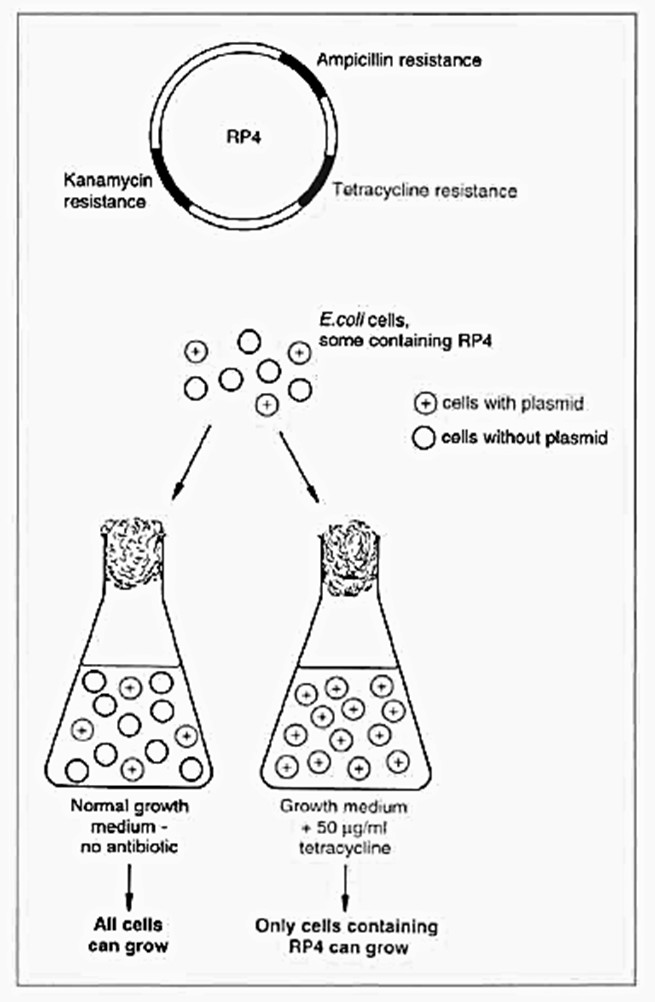
به عنوان مثال : از پلاسمید پروکاریوتی و قطعه ژنی یک DNA نوترکیب ساخته ایم اینرا می خواهیم داخل Ecoli رها بکنیم یکسری آنرا می گیرند بقیه که اکثریت هستند پلاسمید را نمی گیرند برای جدا کردن این دو دسته از آنتی بیوتیکی در محیط کشت استفاده می شود آن دسته از Ecoli ها که پلاسمید را گرفته اند به علت نداشتن ژن مقاوم به آنتی بیوتیک زنده می مانند و بقیه که نگرفته اند کشته می شوند.
3 – حداقل یک Original replication دارند که این شاخص ترین ویژگی پلاسمیدهاست .
مثال : پلاسمید IP 4 که به طور طبیعی در سلول پروکاریوتها است دارای ژنهای مقاوم به آمپی سیلین ، تتراسایکلین و کانامایسین است از همین ویژگی در Select Marker استفاده می شود.
4 - تحمل( Campatibility):
پلاسمیدها Subtype های مختلف دارند و ممکن است به صورت همزمان و طبیعی چندین پلاسمید در داخل یک سلول پروکاریوتی حضور داشته باشد مثلاً بعضی از سویه های Ecoli تا 7 نوع پلاسمید مختلف را در خود جای داده اند .مهم این است که این پلاسمیدهانسبت به هدیگر Campatibility( تحمل) داشته باشند این تحمل, یک سیستم پیچیده ناشناخته است ولی ارتباط ویژه ای با Orginal replication مربوط به هر پلاسمید دارد .
- 5 سایز پلاسمیدها :
سایز پلاسمیدها ازKB 1تا KB250 ( Kilo base = kb ) بطور طبیعی متفاوت است برای کار بیوتیک ، پلاسمیدی مناسب است که زیر kb 10 باشد .
note : هر kb برابر Base chain 1000 است
ویژگی وکتورها :
1 ) توانایی تکثیر داشته باشند . سلول میزبان مرتبط در حال تکثیر است ،اما پلاسمید نو ترکیب آن نتواند تکثیر شود در نتیجه در نسلهای بعدی (سلولهای دختر ) اثری از پلاسمید نخواهد بود لذا اولین و مهمترین ویژگی وکتورها و کلاً پلاسمیدهای نو ترکیبی توانایی تکثیر آنها در داخل سلول میزبان (host ) است .
2 ) داشتن اندازه مناسب برای وکتورها که همان اندازه ای کوچک است.
اگر اندازه پلاسمید بزرگ باشد مشکلاتی را به همراه دارد از جمله :
A :سخت شدن دستکاری ژنتیکی ( Gene manuculation ) روی آن
B : مشکل در ورود آن به host
C : مشکل در پروسه های مختلف مثل خالص سازی ( Plasmid purication ) و ...
مثلاً شکسته شدن در مراحل مختلف انجام کار روی آنها.
لذا باید سایز وکتور مناسب باشد این سایز مناسب در پلاسمید موجود در پروکارپوتها وجود دارد . پلاسمیدها هم سایزهای مختلف دارند یکسری خیلی کوچک هستند که از همان ژنهای transcription کد شونده توسط کروموزوم اصلی پروکارپوت ( در جلسه قبل گفته شده ) استفاده می کنند اما یکسری بزرگ هستند و ممکن است کدهایی را به همراه داشته باشند .
Copy number
تعداد پلاسمیدهای واحد ( از یک نوع ) که در یک زمان ( آنِ واحد ) در یک سلول پروکاریوتی وجود دارد . این تعداد از 15 ، 20 تا 1000 عدد متغیر است این ویژگی مرتبط با Orginal replcation[3] است هر چقدر Orginal repletion قوی تر باشد تمایل تکثیر پلاسمید بیشتر خواهد بود لذا تعداد پلاسمیدهای بیشتر خواهد شد.
ساخت وکتور (پلاسمید مصنوعی ) :
در ساخت وکتورها ، پلاسمیدهای طبیعی پروکاریوتها را به عنوان پایه (base ) قرار داده و پلاسمیدهای مصنوعی را براساس آنها در آزمایشگاه Deve lope می کنیم یعنی با توجه به ویژگیهای مد نظر ، بخشهای مختلفی از پلاسمیدهای طبیعیِ مختلف را جدا کرده و به هم متصل کرده و پلاسمید مصنوعی را می سازند .
این وکتورهای مصنوعی باید خصوصیاتی را همراه داشته باشند :
1 – ژن خاص و مطلوب را داشته باشند.
2 – قابلیت Replication (تکثیر ) داشته باشند .
3 – خاصیت Selection Marker داشته باشند (مثلاً دارا ی ژن مقاوم به آنتی بیوتیک باشند )
4 – بتوانند در رونویسی Transcription و پروتئین سازی Translation پیش روند .
مثال : از اولین وکتورهای که Develope شده است می توان به PBR322 اشاره کرد :
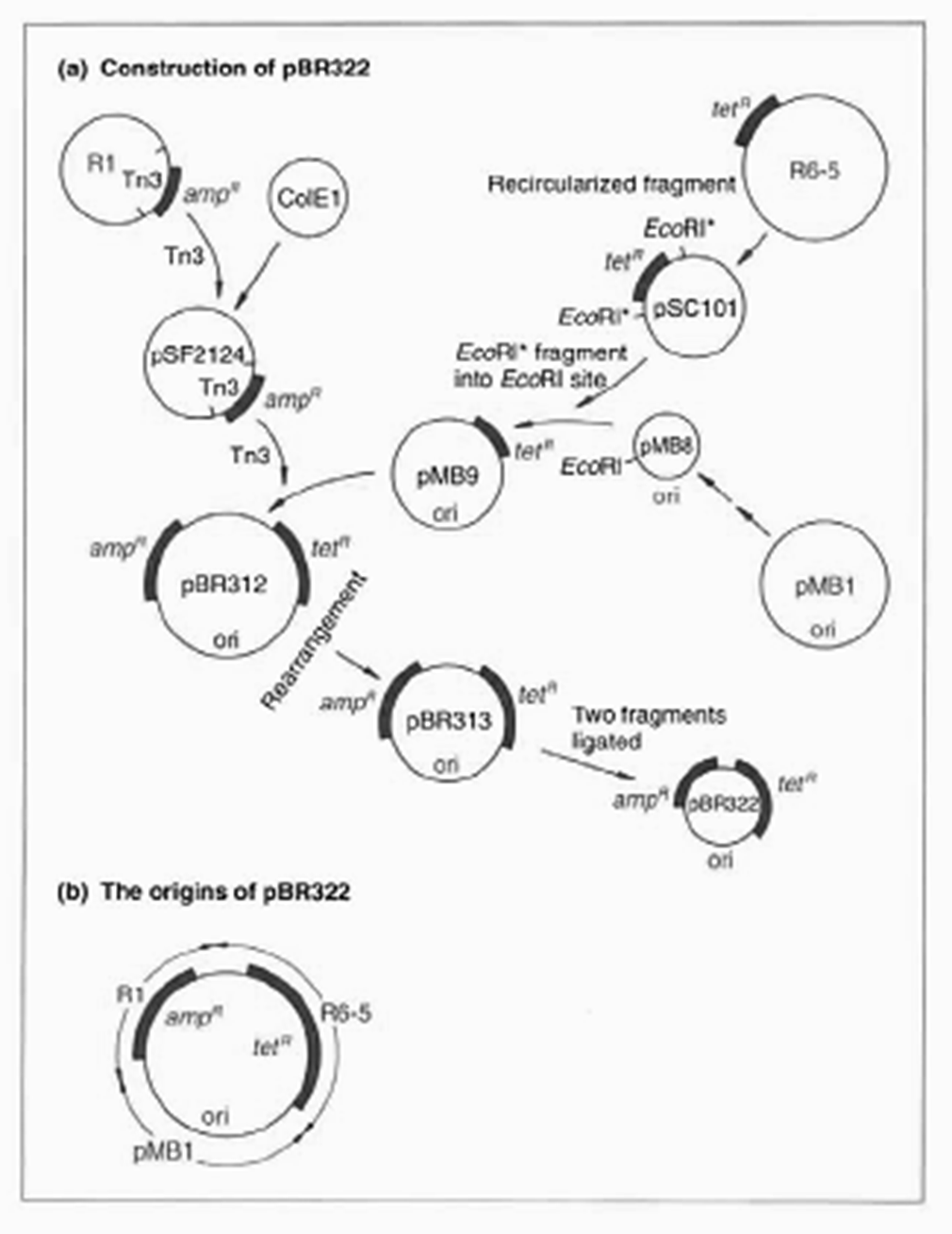
BR: مشخص کننده آزمایشگاهی است که این Developing در آن انجام شده است مثلاً 2 شخص (؟) و ( ؟ ) محقق اصلی آن بودند
322: شماره است که نشان می دهد پس از آن ژنهای مختلف دیگر مثل 325 ، Develope شده است
P: پلاسمید
این پلاسمید از نظر سایز مطلوب است و از جهت[4] Selection Marker هم دارای 2 ژن مقاوم به آمپی سیلین و تتراسایکلین است و هم اینکه high copy number دارد .
با توجه به شکل پلاسمید PBR322 از سه پلاسمید طبیعی موجود در Ecoli ساخته شده است .
1 – ژن مقاوم به تتراسایکلین از پلاسمید R6-5
2 – ژن مقاوم آمپی سیلین از پلاسمید R1
3 – قسمت Orginal replication است از پلاسمید PMB1
(Transcription ) رونویسی پلاسمید سنتتیک :
پلاسمید مصنوعی باید قابلیت رونویسی شدن را داشته باشد در این منظور باید دارای سه جزء اصلی :
1 – Promoter
2– Terminator
3 – Ribosom binding site
Promoter:
ناحیه ای بین( 10 -و 35 -) است (یعنی اولین نوکئوتیدی که رونویسی می شود در این ناحیه حضور دارد ) این سکانسهای واحد ( Consenso cicuances ) در اکثر پروکاریوتها مشابه است تا RNA پلی مراز بتواند همه promoter ها را شناسایی کند . رونویسی از بعد از ناحیه promoter شروع می شود .
RNA پلی مراز با کمک Subunite سیگمای خود, promoter را می شناسد .
Terminator:
ساختار آن در جلسه قبل توضیح داده شده است ( فاصله 10 نوکئوتیدی , حالت سنجاق سری, دم کوتاه پلی A ، پیوندهای سست و جدا شدن RNA m از DNA )
Ribosom bindiy site :
در پروکاریوتها شانگل بارلود (؟) است این ناحیه به Subunite کوچک ریبوزوم متصل شده ،پس از محل ِاتصال ، ناحیه کدون AUG قرار دارد که اسید آمینه متیونین ( اولین اسید آمینه هرزنجیره پروتئینی ) را کد می کند سپس روی RNA m حرکت کرده و تک تک, اسیدهای آمینه را اضافه می کند تا به کدونهای پایانی UAA یا UAG یا UGA برسد . در اینجا سیستم ریبوزم از زنجیره جدا شده و محصول ( زنجیره پلی پپتیدی ) را خواهیم داشت . .
Vectors and hostcells:
وکتورها با توجه به host ارزش و اعتبار پیدا می کنند . لذا با توجه به اینکه چه نوع از host در Gene cloning استفاده می شود نوع وکتور متفاوت می شود . در ساخت وکتور (پلاسمید مصنوعی حاوی قطعه ژنی مد نظر ) باید به پسوندها و پیشوندهایی که همراه قطعه ژنی (همان قطعه ای که می خواهیم کلون کنیم ) دقت شود; مثلاً اگر این قطعه ژنی مربوط به یوکاربوت است با حفظ همان پسوند و پیشوندهای یوکاریوتی اش در یک host پروکارویوتی و حتی host یوکاریوتی نمی تواند بیان شود چون در موجودات مختلف سیستم هایی مانند transcription (رونویسی ) و.... متفاوت است . لذا در طراحی وکتورها باید دقت شود که این وکتور بتواند حاوی یکسری ویژگیهایی باشد که با سیستمهای Replication ، Transcrption و ...ِ میزبان قابلیت تولید محصول را در نهایت داشته باشند . ) باید قطعه ژنی داخل وکتور ،دارای پروموتور قابل خواندن توسط host را باشد(
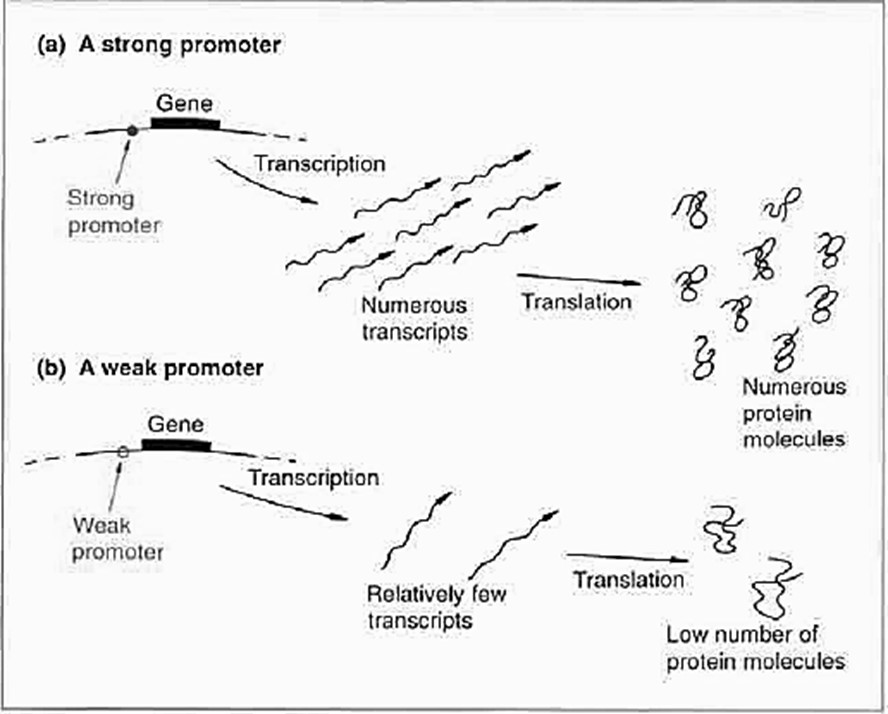
Strong and weak promoters :
همه پروموتورها ناحیه 35 -تا 10- پروموتور را دارند، اما به دلیل تفاوت در یک نوکلوتید، ممکن است Transcription efficacy متفاوتی داشته باشند یعنی سبب تفاوت در تمایل اتصال subunite سیگمای RNA پلی مراز برای اتصال به پروموتورشود و میزان Transcription (رونویسی ) را تغییر دهند پس نقش اصلی در Orginal replication توسط Promoter بازی میشود . اگر وکتوری با Orginal repletion قوی خواستیم ،از یک پروموتور ، ژنی را استخراج می کنیم که به مقدار زیاد در Sorce خود بیان می شود .
از پروموتورهای قابل خواندن در Ecoli می توان به 2 مورد زیر اشاره کرد :
1 – lakky seo promoter
2 – T cell on promoter
Host cells سلولهای میزبان
به ترتیب اولویت :
1 – شاخصترین میزبان پروکاریوتی , Ecoli است .
2 – بعد از Ecoli باسیلوس
3 – رتبه سوم از آنِ مخمرهاست که شاخصترین آنها Saccharomyces cerevisiae
4 – قارچهایی مثل آسپرژیلوس
5 – Mamalion call line یا animal call culturاینها cell line های مختلفی اند که از Original replication های مختلف گرفته شده اند.
مثلاً در مورد سلول کبدی : دارای Cell line : PHG2 ، CHO ، BHK و ..
6 – Transgenic animals
7 – Plant – based expression system (گیاهان متنوع ) :
سیستمهایی که از آنها سلولهای گیاهی به عنوان host مطرح می شوند .
8 – Insect cell wlture system (حشرات )
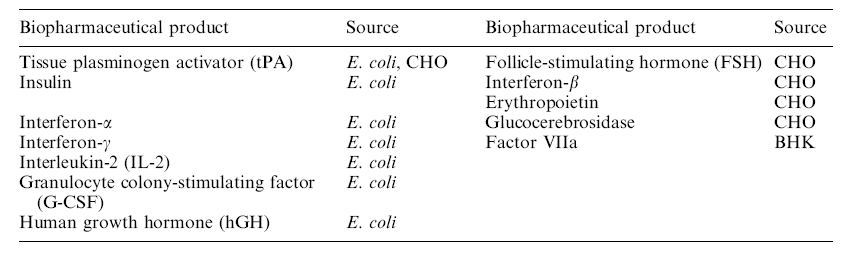
مثالی از میزبانهای فوق : در جدول یکسری ترکیباتی که به صورت Recombinant (نوترکیب ) در داخل میزبانهای مختلف تهیه شده اند را مشاهده می کنید
1 - ( CHO(chinese hamster ovary cell
سلول تخمدان همستر چینی
BHK (body hamster kidney call ) -2
سلول کلیه همستر
Ecoli :
مزیتهای Ecoli برای کسب رتبه اول بین میزبانها :
1 – هزینه : این میزبان در مقادیر خیلی زیاد و با هزینه خیلی کم در سیستم فرمانتوری قابل تولید است و هم اینکه نگهداری از آنها آسان است .
2 – در مدت زمان کوتاهی می توان تعداد زیادی از آنها را داشت این ویژگی مهمی است چون اگر سرعت رشد میزبان پائین باشد سرعت تولید پروتئین هم پائین خواهد بود در نهایت بازده تولید محصول پائین می آید .
3 – معروف است :
مدت طولانی است که به عنوان Cell biologic model در بین پروکاریوتها مطرح بوده است لذا کار با آن راحت است .
4 – تولید میزان بالایی از محصول :
به راحتی دستکاری ژنتیکی می شود .می توان در آن ، سیستمهای پروموتوری را تعبیه کرد که این سیستمها ،تا 30 % کل پروتئین تولیدی در Ecoli را به خود اختصاص دهند لذا بازده تولیدی بالا می رود.
معایب سیستم Ecoli:
– LPS ( lipo poly saccaride ) موجود در cell wall آن ،توکسیک و پاتوژن است .
– عیب دوم برای همه پروکاریوتهاست . پروکاریوتها سیستم اسپلایسینگ ندارند این سیستم که دربوکاریوتها حضور دارد وظیفه اتصال قطعات اگزون به یکدیگر و دور انداختن قطعات ا ینترون را دارد . پس مجبوریم قبل از قرار دادن قطعه ژنی در وکتور ، ژن یوکاریوتی را اسپلایس کنیم ( منظور از اسپلاسینگ یکدست کردن و به هم متصل کردن است )
– Post translation modification (تغییرات پس از ترجمه ) :براساس نوع خاصی از patern (الگو) در هر سلول، این تغییرات که به صورت Acylation و اغلب glycolization (اضافه شدن الیگوساکاریدها به زنجیره پلی پپتیدی ) است رخ می دهد .
نتیجه این تغییرات روی پلی پپتید، در پروکارویوت (میزبان ) سه نتیجه را به همراه دارد :
A : تغییر در خصوصیات فارماکوکینتیک یک پروتئین ( مدت زمان ماندن محصول در بدن و زمان کلیرانس از بدن )
B : اثر روی biological activity پروتئین حاصل : که یا اثر آنرا کم می کند یا اصلاً اجازه نمی دهد محصول اثرگذار باشد از طرفی برای فعالیت برخی از پروتئینها حتماً لازم است مرحله گلیکو لیزاسیون رخ دهد اما متاسفانه طبق الگویی که دریوکاریوتها هست رخ نمی دهد .
C– برخی از پروتئینها برای اثرگذاری دریوکاربوتها لازم نیست که حتماً گلیکولیزه شوند و اگر هم شوند چندان شایان اهمیت نیست مثل 2IL
از موارد A ،B و C نتیجه می گیریم که : ژنی را در Ecoli کلون می کنیم که با گلیکولیزه شدن توسط الگوی پروکاریوتی Ecoli خواص فعالیت بیولوژیکی آن تغییر نکند .
– اکثر پروتئینهای ساخته شده در سیستم Ecoli درون سلولی اند : اگر پروتئین به بیرون ترشح می شد استخراج آن راحتر بود. وقتی پروتئین داخل سلولی باشد درطی Purification ( خالص سازی )، یک مرحله اضافی تر خواهیم داشت چون باید Ecoli را بشکنیم بعد با سانترفیوژهای قوی، پروتئین های داخلش را جدا کنیم لذا خالص سازی سخت تر خواهد شد .
– ساختار سوم پروتئینها تعیین کننده Activity و biological آن است .
این ساختار با تشکیل باند دی سولفیدی S- S بین اسید آینه های گوگرددار مثل سیستئین حاصل می شود که تاخوردگی نهایی پروتئین ( Protein folding) را مشخص می کند متاسفانه در سیستم Ecoli , Protein folding به طورغیر مناسب وجود دارد اما برای فعالیت اکثر پروتئین ها کافی است.
– aggrigation : از نکات مثبت سیستم Ecoli , اختصاص یافتن 30 % کل پروتئین تولیدی، به پروتئینهای ژن خارجی بود . وقتی بار اضافی را به میزبان تحمیل کنیم یعنی مجبورش کنیم که تند تند پروتئین بسازد،همان سیستم folding ضعیف Partial folding )) هم به درستی انجام نمی دهد .
وقتی که یک پروتئین ساختار سوم را به خود می گیرد چون در محیط مایی سیتوپلاسم هست بخش های هیدروفوبی را در داخل وهیدروفیلی را در خارج قرار می دهد و بر این اساس fold می شود .
اما وقتی سیستم folding ضعیف کارکند و قسمت هیدروفوبی را خارج قرار می دهد لذا تداخلات غیر هیدروفونی بین مولکولها ی پروتئین و سیتوپلاسم رخ داده و پروتئینها به هم متصل شده (اگریگه) تولید inclusion body را می کند
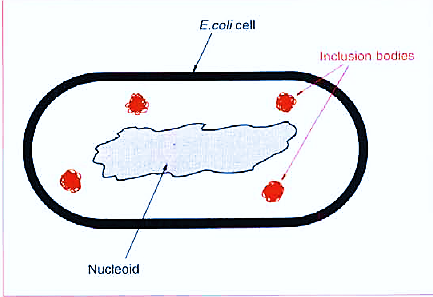
Inclogen bodies:
1 - وقتی پروتئین درون سلولی باشد احتمال تشکیل inclogen bodies هم بیشتر خواهد شد .
2 - مزیت تشکیل inclogen body این است چون دانسیته بیشتری نسبت به سایر اجزای pro داخل Ecoli دارند با سانترفیوژ راحت قابل خالص سازی هستند .
3- پس از خالص سازی ، پروتئین به فرم فعال نیست (راه حل: denaturation یعنی تاخوردگی ها (fold ) را باز کنیم{ساختار سه بعدی را بشکنیم } و مجدداً refold کنیم تا نقاط فعالی که پنهان شده بودند نمایان شوند.)
معایب:
پر هزینه است و ممکن است پروتئینها کاملاً refold نشوند و active site مناسب را پیدا نکنند . راه حل : کلاً از تشکیل in clogene body جلوگیری کنیم به کمک :
1 – بیان کردن ژن در دمای پائینتر از 37 c ( یعنی 30 ): با این کارواکنشهای متابولیکی کندتر شده لذا زمان بیشتر صرف folding
بیشتر و بهتر پروتئین می شود.
2 – استفاده از سویه های Ecoli که مهندسی ژنتیک شده اند و مقادیر زیادی از chaperon protein را در خود تولید می کنند .
پروتئینهای چپرونی وظیفه هدایت پروتئینهای ما را به سوی folding صحیح را دارند تافرم فضایی سوم مناسب را به خود بگیرند
Mamalian cells: (سلول پستانداران )
2 دسته ی پرکاربرد از این سیستم :
1 – CHO
2 – BHK
مزیت :
1- داشتن سیستم اسپلایسینگ
2-ا نجام post transitional modification مطابق با الگوی یوکارپوتی چون پروتئین حاصل از ژن در hust یوکارپوتی تولید میشود لذا گلیکولیزه شدن را مطابق الگوی یوکاریوتی انجام می دهد پس پروتئین دارای Active sites و Biological activit مناسب خواهد بود .
Note( – اگر هدف ما تولید پروتئینی با خواص فارموکوکینتیک مناسب است بهتر است host انتخابی از Mamaliane cell ها باشد
معایب :
1– پیچیده بودن و پر هزینه بودن محیط کشت برای این رده از میزبانها
2 – کند بودن سرعت رشد
3 – نتیجه سرعت کم طولانی تر شدن مدت زمان نگهداری برای تولید پروتئین
4 – حساس بودن به Physical damages (صدمات فیزیکی ) به علت نداشتن cell wall
(مخمرها) : Yeast
نوع پر کاربرد این سیستم : ساکارومیسزسرویزیه
مزیت :
1 – سیستم بیولوژیک و ژنتیکی شناخته شده دارند چون از دیرباز در صنعت تخمیر، ناخودآگاه یا آگاهانه در تهیه پنیر و نان و ... استفاده می شدند .
2 – سیستمهای فرمانتوری شناخته شده دارند ومی توانیم در مقادیر بالا آنها را رشد دهیم و محصول بگیریم .
3 – کم هزینه بودن محیط کشت ( مثل Ecoli )
4 – بالا بودن سرعت رشد ( برخلاف Mamalian cell )
5 – چون جزء یوکاریوتها هستند لذا post transmition modification دارد ( برخلاف Ecoli ) اما patern گلیگولیزه کردن آن با Mamalian cell فرق دارد .
معایب :
1 – متفاوت بودن الگوی posttransmition madification با الگوی لازم
2 – پائین بودن efficacy بیان پروتئین ( در Ecoli از 100 % ، 30 % پروتئینها را پروتیین مد نظر بودند اما در مخمرها 5 % هست )
قارچها fungies
مزیت :
1 – تهیه آلفا آمیلاز یا گلوکوآمیلاز
2 – دارای post transmition modification است.
3 – به علت استفاده دیرینه از آنها بسیار شناخته شده اند .
4 –تولید انبوه در فرمانتورها
5 – تولید پروتئین به صورت extra cellular ï راحت و کم هزینه بودن خالص سازی و سبکتر بودن down stream
معایب :
1 – متفاوت بودن الگوی post transmition modification به علت اضافه شدن زنجیره های الیگومانوزی یا زنجیره های که مانوز، قسمت عمده را تشکیل می دهد ï clearance سریعتر دارند یعنی مدت زمانی که پروتئین در داخل بدن به صورت فعال است کوتاه می شود .
2 – تولید پروتئاز خارج سلولی و دگرده کردن پروتئینها
راه حل: غیر فعال کردن بخش اعظمی از ژنهای بیان کننده ی پروتئازهای قارچی
مبحث انتخاب وکتورها و میزبان تمام شد در ادامه به Gene cloning می پردازیم .
مراحل Gene cloning در صفحه اول جزوه نوشته شده است .
مثال : هدف تولید استرپتوکیناز ( نوعی پروتئین ) است نقش درمانی آن از قدیم الایام به عنوان هضم کننده لخته خونی بوده است .
مراحل تهیه استرپتوکیناز :
1 – ژن تولید کننده این آنزیم در سویه هایی از استرپتوکوکها وجود دارد .
برای افزایش بازده تولید محصول سویه ای را انتخاب می کنیم که بیشترین مقدار استرپتوکیناز را تولید می کند . به این عمل micro organism screening(غربالگری ) گویند بدین منظور سویه های مختلف استرپتوکیناز را رشد می دهیم و سویه ای را انتخاب می کنیم که بیشترین و پر قدرت ترین استرپتوکیناز را تولید می کند .
2 – کشته سویه ی انتخابی استرپتوکوکها : چون نیاز به مقدار زیادی از DNA است لذا سویه ی انتخابی را در محیط کشت رشد می دهیم تا PLATE سلولی تشکیل شود. ( منظور مجموعه سلولی است )
2 نوع محیط کشت داریم :
A : Defind medium مثل M9
B : Complex or undifind medium مثل LB (luria-bertani)
LB هم 2 نوع است:
1 – Brows LB : به فرم مایع است
2 – LB Agar : به فرم جامد است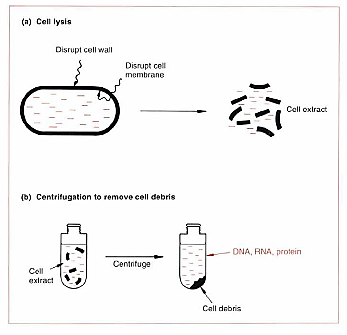
مقایسه A و B:
A : محیط defind :
I - نوع و مقدار هر جزء در محیط مشخص است ( مثلاً مقدار و نوع aa یا نوع منبع کربن و انرژی مشخص است )
II - همیشه این محیط کشت استفاده نمی شود چون گران است
III - اگر بخواهیم M.O[5] در شرایط کنترل شده و خاص کشت شود از این محیط استفاده می شود .
B : محیط undifind :
I -نوع و مقدار هر جزء مشخص نیست
II - ا ساس آن عصاره مخمر ( برای مواد غذایی Nutriants و یونهای Na+ ، k+ ، Mg2+ ) و تریپون ( منبع تولید آمینه اسیدهای مختلف ) است .
برای کشت و تکثیر سویه انتخابی استرپتوکوک از LB brows استفاده میشود . پس از کشت harvesting می کنیم یعنی با سانترفیوژ سلولها را از بقیه اجزاء محیط کشت جدا می کنیم
3 – جدا کردن DNA از کل سلول ( Cell extract) :
باید سلول را بشکنیم. به 2 طریق امکان پذیر است:
A – فیزیکی و B – شیمیایی
AM – فیزیکی : از نیروهای فیزیکی استفاده می شود مثلاً Sonication به کمک sonicator
BM – شیمیایی :
1 - اغلب در آزمایشگاهها از این روش استفاده می شود
II -مثلاً برای استریتوکوک از EDTA ؛ SDS لیزوزیم استفاده می شود بدین طریق ساختار پلی مری پیتدوگلیگان دیواره سلولی باکتری شکسته می شود.
EDTA G[6] :
یک Shelating agent است یونهای دو ظرفیتی (خصوصاً +2Mg ) را به خوبی جذب می کند سبب تغییر در integrity و استحکام cell wall می شود و با جذب
Mg 2+ آنزیمهای DNAase و RNAase که پس از شکسته شدن MO آزاد شده اند را
غیر فعال کند, چون اسید و آنزیم برای فعالیت، Mg2+ لازم دارند
Aلیزوزوم :
سبب تخریب Cell well می شود .
SDS[7] B :
بر خلاف EDTA و لیزووزرم Call wall را تخریب نمی کند بلکه روی غشای سلولی اثر دارد با نفوذ در بین ساختار فسفولیپیدی غشاء با خاصیت دترژانتی خود سبب به هم ریختگی کامل ساختار غشاء می شود .
Note ( : کلاً با EDTA و لیزوزوم به دلیل فروپاشی Cell wall و به دلیل اسمولاریته موجود در محیط خود بخود سلول می ترکد و نقش SDS به عنوان کمک کننده است . حال در محیط Cell debris ( باقی مانده سلولی ) RNA ، DNA و پروتئین داریم .
4- جدا کردن DNA از [8]Contaminants ( Purification : خالص سازی ) :
به 2 روش انجام می شود:
A : دگرده کردن Contaminants
B : Ion exchange chromatography
5 note : قبل از شروع Purification به کمک سانترفیوژ ساده مخلوط پروتئین ، DNA ، RNA را از Cell debrize (چون دانسیته بالایی دارند ته نشین می شوند ) جدا می کنیم
.
: دگرده کردن A : Contminants
از سیستم فنول کلروفرم استفاده می کنیم پروتئینها به راحتی در فنول حل می شوند وقتی محیط با نسبت 1 به 1 فنول کلرو فرم استفاده کنیم, شاهد 2 فازه شدن Cell extrant در دو فاز آبی و آلی فنول کلروفرم خواهیم بود بدین صورت که پروتئین هایی که در
اثر حل شدن دناتوره شده اند بین دو فاز مایی و آلی قرار می گیرند (درمرز) و محیط بالای مرز که فاز مایی است متشکل از DNA , RNA استïپروتئینها جدا شدند
مرحله بعدی جدا کردن RNA و DNA است ï از ریبونوکئاز ( RNAase ) استفاده می کنیم
مزیت : خیلی به صورت روتین این سیستم در آزمایشگاهها به کار می رود چون کم هزینه است
عیب : قدرت خالص سازی پایینی دارد .
B : ION EXCHANGE CHROMATOGRPHY:
-1 ستون که حاوی بستر رزین با بار + است
2 - RNA و DNA زنجیره پلی نوکلئوتیدی منفی هستند ولی DNA ازRNA منفی تر است چون قنددئوکسی ریبوز دارد .
3 - بار پروتئینها فقط در PH (ایزواکتریک ) صفر است
با ریختن مخلوط حاوی DNA و RNA ،PRO ,آنهائی که بار منفی دارند به ستون می چسبند .برای جدا کردنشان، از محلولهای نمکی استفاده می کنیم. هر چقدر غلظت یونهای نمکی بالاتر باشد قدرت بیشتری را برای شکستن پیوند بین مولکول متصل به رزین را دارند و خود در رقابت جایگزین مولکول می شوند .
مرحله اول : که غلظت محلول نمکی کم است پرتئینها جدا می شوند
مرحله دوم : جدا شدن RNA
مرحله سوم : غلظت محلول نمکی بالاست لذا DNA جدا می شود
استخراج پلاسمید :
DNA کرموزومی را برای استخراج ژن لازم داشتیم و پلاسمید را برای ساخت وکتور لازم داریم.
وقتی کروموزوم سلول را جدا می کنیم یعنی غلظتی از DNA و پلاسمید را داریم که برای جدا کردن ایندو باید ببینیم چه تفاوتهایی با هم دارند :
1 – سایز : DNA کروموزومی خیلی بزرگتر است
2 – Conformation
#جداسازی DNA از پلاسمید بر اساس اختلاف در سایز:
1 - وقتی به محیط EDTA و SDS و لیزوزوم اضافه می کردیم سلول میترکید وDNA متصل به غشاء تکه تکه میشد. با اضافه کردن سوکروز به محیط ،محیط هیپرتونیک می شود (افزایش غلظت ) و دیگر سلول نمی ترکد غشاء بازشده در پی جداشدن cell debrise، عده زیادی از DNA کروموزومی هم با آنها خارج می شود .
2- استفاده از 100 X trition به جای SDS : تریتون 100 X یک دترژانت است عامل متلاشی کردن غشاء است اما به خاطر غیریونی بودنش DNA را نمی شکند.
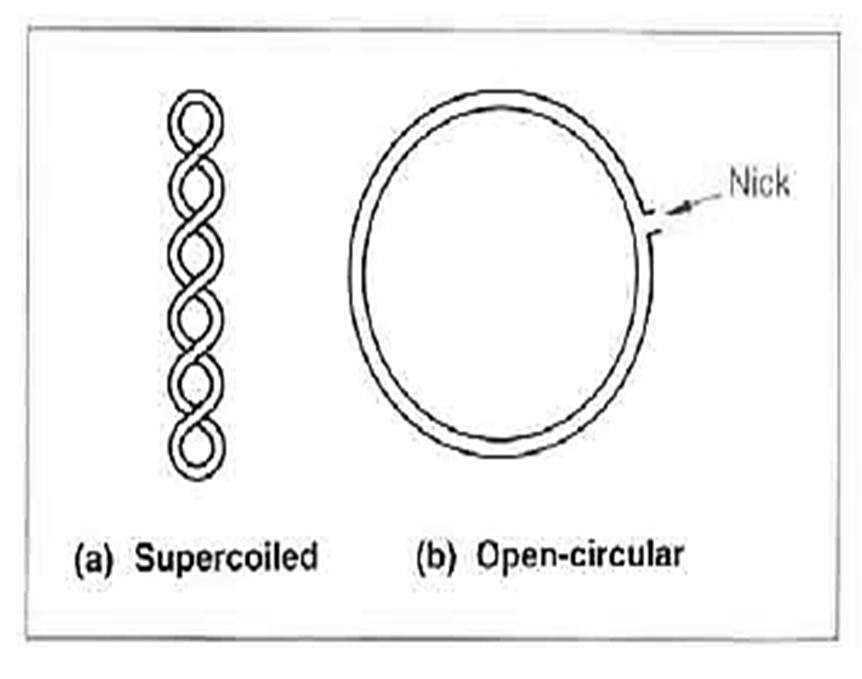
# 2 – جداسازی براساس Conformation :
شباهت DNA و پلاسمید : هر دو حلقوی ، بسته و Supercoil ( به دور خود بپیچد ) هستند.
در پلاسمید اگر بین 2 نوکئوتید آن شکافی ایجاد شود از حالت SUPERCOIL خارج شده و به فرم Relax تبدیل می شود .
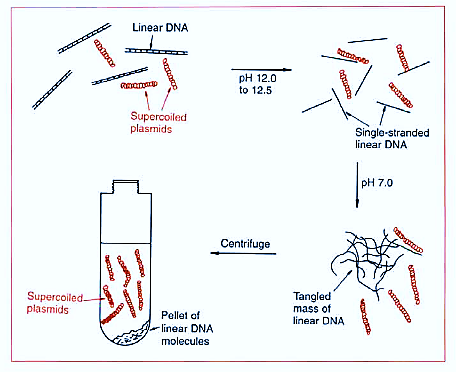
برای کار بیوتک نیاز به پلاسمیدی است که Supercoil باشد بعد از گذشت مدت زمانی از کشت ,MO پلاسمید به این فرم است این زمان در انتهای فاز لگاریتمی است در این حالت میتوان پلاسمید را از DNA جدا کرد چون DNA به صورت خطی و خرد شده در آمده است. لذا PH را به 5/12 – 12 می رسانیم این PH سبب جدا شدن 2 زنجیره DNA خطی می شود اما پلاسمیدی که سوپر کویل است چون خیلی 2 زنجیره به هم نزدیک هستند لذا پیوند هیدروژنی بینشان شکسته نمی شود .
بعد محیط را اسیدی می کنیم سبب Renacharing و تشکیل پیوند هیدروژنی بین قطعات DNA می شود اما به صورت اگریگه اتفاق می افتد چون بدون قانون است و سوپرکویل در محیط اسیدی تغییر نمیکند لذا DNA اگریگه شده به علت دانسیته بالای خود از پلاسمیدهای سوپر کویلی به کمک سانترفیوژ قابل افتراق هستند
مروري بر تكنيكهاي همسانه سازي (Cloning) در پستاندارن
مقدمه:
در روند تكامل، توليد مثل جنسي موجودات عالي به عنوان راهي براي حفظ تنوع ژنتيكي جمعيتهاي انتخاب شده است كه بقاي آن موجود در مواجهه با شرايط مختلف را امكانپذير مي سازد. در اين نوع توليد مثل هر يك از اين نطفه ها حامل نيمي از ژنهاي والدين نر و ماده مي باشد كه به فرزندان منتقل مي شود. تا قبل از كشف روش كلونينگ تصور بر اين بود كه سلولهاي سوماتيك پس از تمايز يافتن قادر به برگشت به حالت اوليه ( تمايز نيافته) نمي باشند. به عبارت ديگر تصور قبلي بر اين پايه بود كه سلولهاي سوماتيك با وجودي كه تنمامي ژنها را در هسته همراه دارند، با اين وجود قادر به توليد موجودي كامل نيستند. كلون كردن به معني تكثير غير جنسي است نمونه عملي آن، تكثير گياهان است و يا در حشراتي مانند زنبور عسل و خزندگان و ماهيها و آبزياني همانند آرتميا پديده اي به نام بكرزائي (Pathenogenis) وجود دارد كه مي توان آن را پديده اي مشابه كلونينگ دانست. كشت بافت گياهي فرآيندي است كه در آن قطعات كوچكي از بافت زنده گياهي جدا شده و به مدت نامحدودي در يك محيط مغذي سترون رشد داده مي شود.كلونينگ از طريق مهندسي ژنتيك در گياهان، حيوانات و يا حتي باكتريها، براي توليد انبوه با كيفيت خاص صورت مي گيرد. از طريق اين تكنولوژي مي توان نسلهاي در حال انقراض را نجات داد. از مزاياي شبيه سازي در پرورش دامهاي اهلي مي توان به استفاده از تعداد محدودي از حيوانات پر توليد با هزينه نگهداري كمتر و افزايش سريع پيشرفت ژنتيكي گله اشاره كرد. با توجه به اينكه فنوتيپ افراد عمدتا تحت تاثير مشترك وراثت و محيط مي باشد هيچگاه حتي در دو قلوهاي يكسان، دو فرد كاملا شبيه به هم نخواهد بود. نتيجتا در شبيه سازي ژنوتيپ افراد كاملا مشابه مي باشد اما دو فرد مذكور فنوتيپ يكساني نخواهد داشت.
روشهاي كلونينگ:
شبيه سازي با روشهاي گوناگوني و با اهداف متفاوت انجام مي پذيرد كه بطور كلي سه روش كلي در اين مورد وجود دارد:
الف- كلونينگ روياني(Embryonic Cloning)
اين روش همان روشي است كه در طبيعت در تولد دوقلوها يا چند قلوها رخ مي دهد. در اين روش در شروع مراحل تقسيم جنيني بعد از لقاح، يعني زماني كه هنوز سلولهاي جنيني تمايز نيافته اند يك سلول را جدا و با تحريكات، اين سلول را به ادامه تقسيم تا حد به وجود آمدن يك جنين مستقل وادار مي كنند.
ب- كلونينگ توليد مثلي(Reproduction Cloning)
هدف از اين روش، توليد موجودات زايا با استفاده از سلولهاي سوماتيك مي باشد. در اين روش در مرحله خاصي از تقسيم سلولي، هسته سلولهاي سوماتيك را كه در هسته شان حاوي تمامي ژنهاي موجود مي باشند جدا كرده و پس از تيمار الكتريكي يا شييميايي اين هسته را در داخل يك تخم لقاح نيافته كه هسته آن قبلا خارج شده قرار مي دهند سپس مجموعه حاصل را در رحم مادري كه بطور مصنوعي شرايط آبستني در آن القاء شده لانه گزيني مي نمايند كه در نهايت موجود جديد كاملا شبيه فردي خواهد شد كه سلول سوماتيك از آن اخذ شده است.
ج- كلونينگ درماني(Therapeutic Clonig)
در اين روش ابتدا با استفاده از سلولهاي سوماتيك يك فرد، شبيه سازي انجام مي گردد و در مرحله اوليه جنيني از روياني كه حاوي چند سلول است تعدادي سلول جدا و در محيط كشت اختصاصي، سلول، بافت يا اندام مورد نظر تكثير مي شود. هدف از اين روش توليد بافت يا عضوي است كه فرد از دست داده است مثل پوست تحليل رفته در نتيجه سوختگي، كليه، كبد، مغز استخوان، قلب، سلولهاي عصبي يا عضلاني. واضح است پيوند اعضا توليد شده به خود شخص، به دليل قرابت ژنتيكي به مراتب موفقيت آميزتر است و بعد از پيوند نيازي به مصرف داروهاي مضرر به منظور جلوگيري از دفع پيوند به مدت طولاني وجود ندارد.
تاريخچه كلونينگ:
تكنيك كلونينگ ابتدا در دوزيستاني مثل قورباغه موفقيت آميز بود. در سال 1996 خبر تولد اولين گوسفند همانند سازي شده مدتها تيتر بسياري از نشريات و منابع خبري را به خود اختصاص داد. مبناي علمي اين خبر در سال 1997 در يك مقاله چاپ شده در مجله نيچر تحت عنوان» توليد نتاج زنده حاصل از سلولهاي جنسي و سلولهاي بالغ پستانداران« به اثبات رسيد. اين گوسفند ماه از سلولهاي پستاني منجمد يك گوسفند كه سالها پيش مرده بود، بدست آمد. در بوجود آوردن دالي دانشمندان با جدا سازي 227 سلول از سلولهاي پستان گوسفند بالغ و انتقال آن به 227 تخمك غير بارو كه هسته آنها خارج شده بود توانستند سلولهاي جنيني بوجود آوردند و آنها را به مدت 6 روز در آزمايشگاه كشت دادند. دانشمندان سپس 29 سلول جنيني را كشت داده و به 29 ميش جانشين به عنوان مادر دوم وارد كرده و در رحم لانه گزيني نمودند در نهايت فقط يكي از آنها توليد گوسفند زنده به نام دالي كرد كه بعد از 5 ماه و نيم از دالي متولد شد.
در حقيقت دالي دوقلوي يكسان همان گوسفندي بود كه مدتها پيش مرده بود. نژاد گوسفند دالي از نژاد فين دورست بود و نام آن از خواننده معرف دالي پاترن گرفته شده بود. زمان تولد دالي 5 جولاي 1996 بود كه با وزن تولد 5/6 كيلو در موسسه رازلين اسكاتلند متولد شد. در نتيجه آميزش طبيعي دالي با يك قوچ نژاد ولش مانتيشن كه ديويد نام داشت در آوريل 1998 يك بره به نام Bonnie متولد شد و در طول زندگي دالي توانست شش بره سالم را بدنيا آورد. در همان سن 6 سالگي مشخص شد كه دالي مبتلا به فرسودگي مفاصل و پيري زود رس شده است از آنجاييكه گوسفند معمولا مي تواند 12 تا 13 سال زندگي كند اين سوال مطرح شده كه چرا دالي در حالي كه شش سال داشت به بيماري مختص دوران كهولت گوسفندان مبتلا شده است. در 14 فبريه 2003 به حيات اين گوسفند به علت بيماري عفونت شش و جراحات كشنده ناشي از اين بيماري خاتمه داده شد. ايان ويلموت سرپرست تيم بوجود آورنده دالي، ابراز نمود كه عفونت شش يك عارضه معمولي در گوسفنداني است كه به مدت طولاني در اصطبل نگهداري مي شوند و با احتمال مساوي امكان بروز اين عارضه در گوسفندان غير همانند سازي شده قابل انتظار است. ويلموت در ادامه سخنان خود افزود كه احتمالا دالي اين بيماري را از گوسفندان ديگري كه همراه او در اصطبل نگهداري مي شدند گرفته بود. در هنگام مرگ دالي شش سال داشت پس از مرگ پيكر دالي در موزه بين المللي اسكاتلند نگهداري شد و در معرض ديد عموم در شهر ادينبورگ قرار گرفت.يك سال پس از تولد دالي، در سال 1998 اولين موشهاي همانند سازي شده و طي سالهاي 1999 الي 2000 اولين خوك، بز و گاو همانند سازي شده با موفقيت به دنيا آمدند. اولين قاطر كلون شده در 5 مه 2003 توليد گرديد و با اين تولد اميد به موفقيت در كلون كردن آتي اسبهاي مسابقه افزايش يافت. دانشمندان دانشگاه آيداهو با قرار دادن DNA سلول پوست يك قاطر به درون تخمك تخليه شده، يك اسب به تولد رساند. يانگ يانگ بز همانند سازي از يك سلول سوماتيك مي باشد كه توسط دانشمندان چيني بوجود آمده است. در همانند سازي اين بز از تكنيكي به نام انتقال هسته استفاده شد. در اين تكنيك از سلولهاي گوش يك بز بالغ و از سلولهاي تخمك بزهاي ديگر نمونه گيري و كشت سلولي انجام شد. بز يانگ يانگ از طريق اميزش طبيعي با يك بز نر 6 ساله موفق به توليد دو بزغاله با جنسيت نر و ماده شد كه تا كنون گفته مي شود هر دو بز از لحاظ سلامتي در وضعيت مناسبي به سر مي برند.در 27 دسامبر سال گذشته شركت كلونايد به عنوان نخستين موسسه فعال در زمينه Human Cloning كه در سال 1997 ميلادي توسط فرقه اي بنام رايليان به رهبري فردي بنام Claude Vorihon مشهور به دايل تاسيس گرديد ادعا كرد اولين انسان همانند سازي شده را بوجود آورده است.اين فرقه با افكار عجيب خود معتقدند كه انسان بر روي زمين توسط موجودات ساير كرات از طريق روشهاي مهندسي ژنتيك بوجود آمده است. ا ولين انسان كلون شده كه توسط اين شركت پا به كره خاكي گذاشته، دختري است كه زيركانه به نام حوا(Eve) براي او انتخاب گرديده و از يك زن 31 ساله آمريكايي نشات گرفته است. منشا اين دختر يك سلول از كودك دو ساله اي بود كه در يك سانحه رانندگي جان باخته است. هنوز آزمايش DNA بر روي كودك صحت ادعا را ثابت نكرده است.
مزايا و معايب كلونينگ
حيوانات كلون شده اجازه پيشرفت سريع در درك مكانيزم روشن و خاموش كردن ژنها را مي دهد و بوسيله استفاده از حيوانات همانند سازي شده و يكسان از لحاظ ژنتيكي دانشمندان قادرند نتياج سريع و دقيقي را بدست آوردند چرا كه تفائت ژنتيكي در اين موجودات به حداقل ممكن خود رسيده است. از ديگر مزاياي اين تكنيك، كلونينگ سلولهاي حيواني اينست كه به ما اجازه مي دهد كه گونه هايي از موجودات زنده را كه در خطر انقراض قرار دارند را نجات دهيم.
از اهداف كلونينگ در آزمايشگاههاي كشورهاي مختلف مي توان به امكان بازيابي جواني، كمك به پيشگيري حملات قلبي، استفاده از سلولهاي بنيادي براي ترميم سلولهاي مغز و بافتهاي سوخته ، درمان نازايي، درمان ژنهاي معيوب، درمان سرطان و كاربردهاي محرمانه نظامي اشاره نمود.
از معايب اين روشها اينست كه دانشمندان هنوز به حيات طولاني مدت و سلامت حيوانات كلون شده اطمينان ندارند. اين به دليل آن است كه سلولهايي كه عمر بالايي دارند و در معرض اشعه تميار مي شوند ممكن است حاوي جشهااي مضرر در ژنوم شوند. بعضي متخصصان بر اين باورند كه با وجودي كه گله هاي يكسان حاصل از كلونينگ توليد مناسبي را خواهند داشت اما به علت كاهش شديد تنوع امكان هر نوع نتايج غير قابل پيش بيني وجود خواهد داشت. در نهايت اعداد و ارقام ناشي از همانند سازي نيز همواره نشان مي دهد كه احتمال موفقيت در همانند سازي در بهترين حالت 5 الي 10 درصد مي باشد و در حدود 75 درصد كلونها در دو ماه اول زندگي از بين مي روند. دستيابي به تكنيكهاي اين روش به دست بزهكاران نيز تهديد جدي و نگران كننده عمده اي است كه ممكن است جهان را با نابودي مطلق روبرو كند.
جمع بندي:
كلون كردن به معني تكثير غير جنسي است.كلونينگ از طريق مهندسي ژنتيك در گياهان، حيوانات و يا حتي باكتريها، براي توليد انبوه با كيفيت خاص صورت مي گيرد. از طريق اين تكنولوژي مي توان نسلهاي در حال انقراض را نجات داد. از مزاياي شبيه سازي در پرورش دامهاي اهلي مي توان به استفاده از تعداد محدودي از حيوانات پر توليد با هزينه نگهداري كمتر و افزايش سريع پيشرفت ژنتيكي گله اشاره كرد. از اهداف كلونينگ در آزمايشگاههاي كشورهاي مختلف مي توان به امكان بازيابي جواني، كمك به پيشگيري حملات قلبي، استفاده از سلولهاي بنيادي براي ترميم سلولهاي مغز و بافتهاي سوخته ، درمان نازايي، درمان ژنهاي معيوب، درمان سرطان و كاربردهاي محرمانه نظامي اشاره نمود. در بهمن ماه 1381 انجمن ژنتيك ايران طي بيانه اي ضمن تاكيد بر حقوق اساسي انسانها و احترام به خانواده و حقوق آن به عنوان بنيادترين نهاد مدني، كاربرد صحيح و قانونمند دستاوردهاي علمي چون كلونينگ در راستاي بهبود درماني و سلامت انسان را لازم دانست.
فیلم آموزش کلونینگ ارائه شده توسط دانشکده علوم سلولی مولکولی دانشگاه سیدنی (زبان فیلم انگلیسی)
♦♦♦ در صورت داشتن هرگونه سوال در مورد این موضوع برای ما نظر بگذارید (در پایین همین صفحه). در اسرع وقت به تمامی سوالات شما توسط کارشناس مربوطه پاسخ داده خواهد شد. با تشکر ♦♦♦
مطالب مشابه :
- اصول PCR و کاربردهای آن، طراحی پرایمر
- دستگاه فرمانتور | بیوراکتور چیست؟
- کامل ترین مجموعه کروماتوگرافی |انواع و روشهای کروماتوگرافی| بیوتکنولوژی
- بهینهسازی تولید | طراحی آزمایشها با روش متدولوژی سطح پاسخ (RSM)
- معرفی تجهيزات آزمايشگاهی
- رفع اشکال تخصصی روش بلاتینگ نیمه خشک (سمی درای) | بیوتکنولوژی
- آموزش قدم به قدم طراحی ازمایش (RSM) | با نرم افزار دیزاین اکسپرت +نحوه ارائه در مقالات علمی و پایان نامه ها
- رفع اشکال تکنیک وسترن بلات(Western blot)|بصورت کامل و تخصصی | بیوتکنولوژی
- طراحی آزمایش چیست؟ | آموزش کلیات به همراه توضیحات کامل هر مرحله
- آموزش RSM| تحلیل نمودارهای آماری در روش سطح پاسخ | نرم افزار دیزاین اکسپرت

دیدگاهها