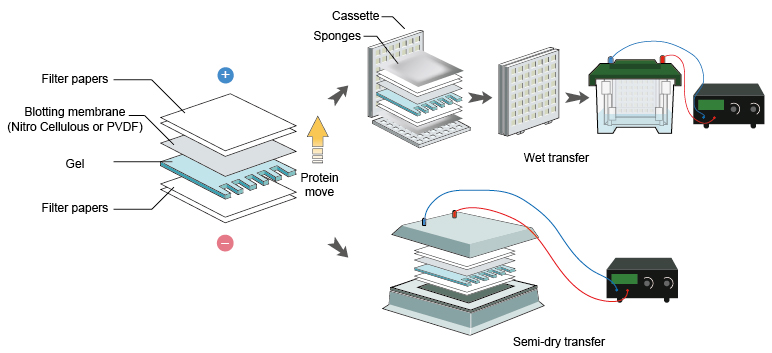
انتقال پروتئین به روش سمی درای
مطالب مرتبط:
وسترن بلات(Western blot) |توضیح کامل تئوری و مراحل عملی|بیوتکنولوژی
رفع اشکال تکنیک وسترن بلات(Western blot)|بصورت کامل و تخصصی | بیوتکنولوژی
رفع اشکال تخصصی روش بلاتینگ نیمه خشک (سمی درای) | بیوتکنولوژی
توضیح کامل تکنیک SDS-PAGE + رفع اشکال تکنیک الکتروفورز عمودی
برای انتقال پروتئین ها در این روش به تانک بافر نیازی نیست و ارتباط غشا و ژل با الکترودها که به شکل صفحه هستند، از طریق چند لایه کاغذ خیس فراهم میشود. اطلاق لفظ نیمه خشک به این روش نیز به همین خاطر است. انتقال نیمه خشک معمولا ساده تر و سریع تر از روش انتقال تر است و به مقدار بسیار کمی بافر نیاز دارد. محدودیت ذخیره بافری به نوبه خود باعث می شود که با این روش نتوان بلاتینگ را بیش از ۲ ساعت طول داد. در غیر اینصورت بهتر است، انتقال به روش تانک صورت گیرد.
در انتقال به روش نیمه خشک امکان بلاتینگ ۶ ژل به صورت همزمان وجود دارد. در این حالت هر ساندویچ ژل با ورقه دیالیز (سلوفان) از ساندویچ بالا یا پایین جدا می گردد. در این روش نیم توان ژل های مختلف را روی هم قرار داد و به طور همزمان بلات نمود. در حالتی که بلاتینگ در یک ژل صورت می گیرد، امکان استفاده از سیستم بافری پیوسته یا ناپیوسته وجود دارد. انتخاب بافر مناسب بستگی به ماهیت پروتئین، نوع الکتروفورز، نوع غشای مورد استفاده و خصوصیات ژل دارد.
انتقال نیمه خشک در بافر پیوسته
بافرهای پیوسته مورد استفاده در انتقال نیمه خشک معمولا ترکیبی از تریس-گلیسین با قدرت یونی و PH متفاوت هستند که بسته به شرایط آزمایش، ممکن است حاوی غلظت بسیار کمی از SDS باشند. تعدادی از این بافرها در جدول زیر آمده است. می توان این بافرها را به روش نیمه خشک نیز استفاده کرد.
| نام بافر | اجزای سازنده | PH | توضیحات |
| بافر تاوبین | تریس ۲۵ میلی مولار، گلیسین ۱۹۲ میلی مولار، متانول ۲۰ ٪ (V/V) | ۸٫۳ | اولین بافری که برای الکتروبلات ارایه شد. |
| بافر تاوبین داری SDS | تریس ۲۵ میلی مولار، گلیسین ۱۹۲ میلی مولار، متانول ۲۰ ٪ (V/V)، SDS 0.05 درصد وزنی حجمی | ۸٫۳ | SDS شدت بار منفی و حلالیت پروتئین ها را بالا می برد ولی از عوامل مزاحم در اتصال پروتئین ها به غشا است در صورت لزوم می توان از غلظت های کمتر آن استفاده کرد. |
| بافر تاوبین رقیق شده | تریس ۱۲٫۵ میلی مولار، گلیسین ۹۶ میلی مولار، متانول ۱۰ درصد (حجمی/حجمی) | ۸٫۳ | به دلیل قدرت یونی کمتر، گرمای کمتری در طی انتقال تولید می شود. ظرفیت بافری آن نیز محدودتر است. |
| بافر تاوبین تغییر یافته دارای SDS | تریس ۳۹ میلی مولار، گلیسین۴۸ میلی مولار، متانول ۲۰ درصد (حجمی/حجمی)، SDS 0.03 درصد (وزنی/حجمی) | ۹٫۵ | به دلیل وجود SDS و PH بالاتر، انواع پروتئین های الکتروفورز شده با SDS-PAGE و ایزوالکتریک فوکوسینگ را منتقل می نماید. |
| بافر اسکافر-نیلسن | تریس ۴۰ میلی مولار، گلیسین ۳۹ میلی مولار، متانول ۲۰ درصد (حجمی/حجمی) | ۹٫۲ | PH آن بالاتر از بافر تاوبین است و قدرت یونی ضعیف تری دارد. |
| بافر تاوبین بدون متانول | تریس ۲۵ میلی مولار، گلیسین ۱۹۲ میلی مولار | ۸٫۳ | در انتقال گلیکوپروتئین های بزرگ می توان از آن استفاده کرد. |
| بافر CAPS | CAPS 10 میلی مولار، متانول ۱۰ درصد (حجمی/حجمی) | ۱۱ | در الکتروبلات به هدف تعیین توالی اسیدهای آمینه در پروتئین مناسب است. |
جدول ۱) انواع بافرهای پیوسته مورد استفاده در الکتروبلاتینگ
مواد مورد استفاده جهت آزمایش
- بافر انتقال. این بافر شامل تریس ۱۲٫۵ میلی مولار، گلیسین ۹۶ میلی مولار، SDS03 درصد و متانول ۱۰ درصد با PH/8.3 می باشد. برای تهیه آن ۱٫۵ گرم تریس باز، ۷٫۲ گرم گلیسین و ۰٫۳ گرم SDS را در حدود ۸۰۰ میلی لیتر آب مقطر حل کنید. ۱۰۰ میلی لیتر متانول اضافه کنید، حجم نهایی محلول را با آب مقطر به ۱ لیتر برسانید. محلول هنگام استفاده باید خنک باشد.
- غشای نیتروسلولز با اندازه منافذ ۰٫۴۵ میکرون یا PVDF.
- کاغذ واتمن ضخیم یا کاغذ الکتروفورز
روش انجام آزمایش
- مقداری بافر انتقال در یک ظرف تمیز بریزید. ژل را پس از برداشتن قسمت بالای آن (قسمت متراکم کننده) در بافر قرار دهید.
- ۶ لایه کاغذ صافی و یک لایه غشا به اندازه ژل ببرید و در ظرف بافر خیس کنید. اگر از غشای PVDF استفاده می کنید، ابتدا آن را چند لحظه در متانول خالص خیس کنید و سپس در بافر قرار دهید. از تماس دست با اجزای بلات و محلول ها خودداری کنید.
- صفحه آند ( با سیم قرمز) را در محل مربوطه در تانک الکتروفورز قرار دهید. ابتدا ۲-۳ لایه کاغذ خیس شده در بافر روی آند قرار دهید. سپس بقیه اجزا را مطابق شکل زیر روی هم بچینید. بعد از قرار دادن هر لایه، با پیپت یا لوله آزمایش تمیز به عنوان غلتک حباب های هوای احتمالی را خارج کنید.
- صفحه کاتد را روی مجموعه بلاتینگ قرار دهید. سپس ۱-۲ ساعت در ولتاژ ۲۰-۳۰ ولت الکتروفورز نمایید.
رنگ آمیزی عمومی پروتئین ها در غشا
| ماده رنگ آمیزی | حساسیت (میکروگرم در باند) | نوع غشا |
| فاست گرین FG | ۵/۱< | نیتروسلولز، PVDF |
| پانسو-اس | ۵/۱< | نیتروسلولز، PVDF |
| کوماسی آبی R-250 | ۵/۱ | PVDF |
| آمیدوبلک ۱۰B | ۵/۱ | نیتروسلولز، PVDF |
| جوهر هندی | ۱/۰ | نیتروسلولز، PVDF |
| آهن کلوئیدی | ۰۳/۰ | نیتروسلولز، PVDF و نایلون |
| بیوتین و آویدین-پراکسیداز | ۰۳/۰ | نیتروسلولز، PVDF و نایلون |
| طلای کلوئیدی | ۰۰۴/۰ | نیتروسلولز، PVDF |
جدول ۲) موادی که برای رنگ آمیزی عمومی پروتئین ها در غشا بکار می روند.
بعد از بلاتینگ پروتئین ها لازم است اطلاعاتی در مورد کیفیت و کمیت باندهای انتقال یافته بدست آید، یا پروتئین خاصی به هدف مطالعات بعدی (مثلا تعیین توالی) مشخص گردد.
برای این کار می توان غشای نیتروسلولز یا PVDF را با مواد مختلف رنگ امیزی نمود . رنگ آمیزی پروتئین ها بسته به هدف آزمایش ممکن است به صورت قابل برگشت و یا غیر قابل بزگشت باشد. پانسو-اس، جوهر هندی، آمیدوبلک و کوماسی آبی از مواد متداول برای رنگ آمیزی عمومی پروتئین ها در غشا هستند. رنگ آمیزی ژل نیز کامل یا ناقص بودن انتقال پروتئین ها را نشان می دهد. باندهای پروتئین در ژل و غشا دقیقا هم موقعیت نمی باشند، زیرا ژل در طی متعادل سازی در محلول انتقال به دلیل وجود متانول ، مقداری کوچک می شود.
رنگ آمیزی قابل برگشت با پانسو- اس
محلول رنگ آمیزی شامل پانسو-اس ۱/۰ درصد وزنی- حجمی در اسید استیک ۵ درصد حجمی -حجمی است. محلول اماده آن نیز توسط شرکت های مختلفی عرضه می شود. برای رنگ امیزی غشا را به مدت ۵-۱۰ دقیقه در مقدار کافی محلول رنگ قرار دهید. سپس با آب مقطر بشویید تا زمینه غشا بی رنگ گردد.
باندهای پروتئینی بعد از رنگ امیزی به رنگ قرمز در می آیند. اگر شستشو با آب ادامه یابد، باندها نیز بی رنگ می گردند. رنگ امیزی با پانسو-اس دخالتی در تشخیص باندها به روش اختصاصی (مثلا ایمونوبلاتینگ) یا در تعیین توالی اسیدآمینه ها ندارد. حساسیت این روش نشبتا پایین می باشد.
رنگ آمیزی قابل برگشت با آمیدوبلک
محلول رنگ امیزی شامل آمیدوبلک با غلظت ۰۱/۰ درصد وزنی –حجمی در آب مقطر می باشد. برای رنگ آمیزی، غشا را ۲۰-۳۰ دقیقه در مقدار کافی محلول رنگ قرار دهید. سپس با آب بشویید تا زمینه غشا بیرنگ گردد. رنگ باندهای پروتئینی به تدریج ضعیف و بالاخره ناپدید می شود.
رنگ آمیزی غیر قابل بازگشت با کوماسی بلو
محلول رنگ امیزی شامل کوماسی بلو R-250 با غلظت ۱/۰ درصد وزنی حجمی در محلول اسید استیک ۷ درصد حجمی-حجمی و متانول ۵۰ درصد حجمی-حجمی در آب مقطر است.
محلول رنگ بر شامل اسید استیک ۷ درصد و متانول ۵۰ درصد در آب مقطر است. رنگ امیزی ژل با کوماسی بلو نیز با همین محلول ها صورت می گیرد.
غشا را ۱۵ دقیقه در مقدار کافی محلول رنگ قرار دهید. محلول رنگ را تخلیه کرده، غشا را در محلول رنگ بر بشویید تا زمینه آبی آن بی رنگ گردد. سپس غشا را در آب مقطر بشویید.
کوماسی بلو برای رنگ آمیزی پروتئین ها در PVDF مناسب است. این نوع رنگ را برای رنگ آمیزی نیتروسلولز بکار نبرید. زیرا زمینه آن شدیدا رنگی می شود.
رنگ آمیزی غیر قابل برگشت با آمیدوبلک
محلول رنگ آمیزی شامل آمیدوبلک آمیدوبلک ۵/۰ درصد وزنی حجمی، اسید استیک ۵ درصد حجمی-حجمی و متانول ۵۰ درصد حجمی-حجمی در آب مقطر است.
محلول رنگ بر شامل اسید استیک ۵ درصد و متانول ۵۰ درصد در آب مقطر است.
غشا را ۵ دقیقه در محلول رنگ بر قرار دهید. محلول رنگ آمیزی را تخلیه کنید و غشا را با محلول رنگ بر بشویید تا زمینه آبی رنگ شود.
رنگ آمیزی مارکرهای پروتئینی
تعیین برخی از خصوصیات پروتئین ها همچون اندازه یا نقطه ایزوالکتریک (PI) با استفاده از مارکر های پروتئینی صورت میگیرد. برای تشخیص مارکرها در غشا می توان از روش های زیر کمک بگیرید.
- قسمت مربوط به مارکرها را از بقیه غشا جدا نمایید و با یکی از روشهای غیر قابل برگشت که در صفحات قبل به آنها اشاره شد، رنگ آمیزی نمایید (PVDF را با کوماسی و نیتروسلولز را با آمیدوبلک رنگ کنید.)؛ سپس این بخش از غشا را خشک نمایید و در کنار بقیه نتایج قرار دهید.
- بسته به نوع برند موقعیت مارکرها و تعداد باندشان متفاوت است.
- می توان شکل بیوتینه شده مارکرها را تهیه کرد و یا مارکرها را در آزمایشگاه به بیوتین متصل نمود. تحت چنین شرایطی با در اختیار داشتن کونژوگه آویدین-پراکسیداز یا آویدین و کونژوگه آنتی آویدین-پراکسیداز می توان موقعیت مارکرها را مشخص نمود.
- آلبومین مرغی و آلبومین گاوی از پروتئین هایی هستند که در بسیاری از انواع مارکرها وجود دارند. با در اختیار داشتن آنتی بادی ضد این دو پروتئین به صورت کانژوگه با آنزیم (یا آنتی بادی ضد آنها و آنتی بادی ثانویه کانژوگه) می توان موقعیت آنها را در غشا تعیین ساخت. این روش زمانی قابل اجرا است که از این پروتئین ها به عنوان ماده مسدود کننده در غشا استفاده نشود.
تشخیص اختصاصی پروتئین ها در غشا
تتشخیص یا رنگ آمیزی اختصاصی باندهای پروتئینی در غشا، بر پایه واکنش آنها با لیگاندهای اختصاصی صورت می گیرد. برای انجام این کار مولکول های لیگاند را به طور مستقیم (اولیه) و یا غیر مستقیم (ثانویه) با مواد رادیواکتیو، فلورسانس، مواد رنگی یا آنزیم ها نشان دار می کنند و با کمک آنها به تشخیص اختصاصی پروتئین ها می پردازند. آنتی بادی ها از پر استفاده ترین لیگاندهای اختصاصی هستند که به اهداف مختلف تشخیص اختصاصی پروتئین ها می پردازند. آنتی بادی ها از پر استفاده ترین لیگاندهای اختصاصی هستند که به اهداف مختلف تشخیصی یا پژوهشی به کار می روند. اساس روش ایمونوبلاتینگ که اهمیت آن بر محققین علوم زیستی آشکار است، موید چنین ادعایی است.
تکنیک وسترن بلاتینگ
این روش که به ایمونوبلات نیز معروف است بر پایه واکنش اولیه آنتی بادی-آنتی ژن می باشد. در این روش پس از بلاتینگ پروتئین ها، ابتدا مناقط آزاد غشا مسدود می شود (مرحله بلوکه کردن). سپس شرایط واکنش آنتی بادی (برای مثال سرم بیمار) با باندهای پروتئینی فراهم می گردد و به دنبال آن ، با استفاده از ماکرومولکول های نشان دار (برای مثال آنتی بادی ضد ایمونوگلوبولین انسان که به آنزیم متصل است) نتیجه واکنش اولیه معلوم می گردد. امروزه وسترن بلاتینگ را به طور گشترده در تشخیص طبی و تحقیقات بکار می برند. اگرچه انجام این روش تابع یک سری اصول کلی است، با این حال شرایط و جزئیات آن وابسته به هدف آزمایش است.
مرحله مسدود سازی
غشاهای مورد استفاده در بلاتینگ ظرفیت زیادی برای گرفتن پروتئین ها دارند (برای مثال ۱۰۰ میکروگرم در هر سانتیمتر مربع از غشای نیتروسلولز) دارند. این خصوصیت اگرچه در جای خود بسیار مطلوب است ولی با اتصال غیر اختصاصی پروتئین های نشان دار در مراحل بعدی آزمایش به بروز اختلال در تشخیص منجر می شود. از این رو باید مناطق آزاد غشا قبل از مراحل تشخیص مسدود گردد. بهترین راه مسدود کردن این مناطق آزاد استفاده از پروتئین هایی است که خود با مواد نشان دار (مثل آنتی بادی) واکنش نمی دهد. کم هزینه بودن و سهولت تهیه از معیارهای اصلی انتخاب پروتئین مسدود کننده است. در جدول زیر نام و غلظت کاری تعدادی از پروتئین های مسدود کننده آمده است. دترجنت ها نیز می توانند از اتصال پروتئین ها به غشا جلوگیری کنند.توین-۲۰ معمولترین دترجنت مورد استفاده در این کار است. باید این نکته را توجه کرد که توین -۲۰ در غلظت های بالا (بیش از نیم درصد) در پاره ای موارد از اتصال لیگاند به پروتئین نیز جلوگیری میکند.
| ماده مسدود کننده | توضیحات |
| آلبومین سرم گاو | در غلظت ۲-۵ درصد در بافر (معمولا PBS) برای ۱-۲ ساع بکار می رود. برای مسدود کردن نایلون غلظت ۱۰ درصد آن به مدت ۱۲-۱۶ ساعت لازم است. |
| شیر خشک بدون چربی | در غلظت ۳ درصد بکار می رود. بسیار ارزان است. بدلیل محتوای قندی زیاد از اتصال لکتین ها یا آنتی بادی های ضد کربوهیدرات (به عنوان مولکول های نشان دار) جلوگیری می نماید |
| آلبومین مرغ | در غلظت ۱ درصد بکار می رود. |
| ژلاتین | در غلظت ۳/۰-۳ درصد بکار می رود. ژلاتین ماهی خصوصیات مناسب تری نسبت به ژلاتین پستانداران به عنوان ماده مسدود کننده دارد. |
| دترجنت (توین-۲۰) | غلظت بین ۱/۰-۰۵/۰ درصد آن کافی است. راحت و کم هزینه است. از واکنش های غیر اختصاصی بین پروتئین ها نیز جلوگیری می کند. |
جدول ۳) انواع مسدود کننده مورد استفاده در بلاتینگ
تشخیص با آنتی بادی
پس از بلاتینگ پروتئین ها و بلوکه کردن غشا، مرحله تشخیص اختصاصی را می توان انجام داد. همان گونه که قبلا نیز گفته شد ایمونوبلاتینگ در بسیاری از موارد به هدف تشخیص طبی است. در این موارد باندهای انتقال یافته شامل همه یا بخشی از پروتئین های پیکره میکروب (باکتری، ویروس یا قارچ) است که وجود یا عدم وجود آنتی بادی ضد سرم آنها در سرم انسان یا حیوان بررسی می گردد. شناسایی با استفاده از آنتی بادی ها مانند تکنیک الایزا به دو روش صورت می گیرد: مستقیم و غیر مستقیم. در تکنیک مستقیم آنتی بادی اولیه که جهت تشخیص آنتی ژن مورد استفاده قرار می گیرد، با استفاده از یک آنزیم و یا رنگ فلوئورسنت نشان دارد شده است. اما در تکنیک غیرمستقیم، ابتدا یک آنتی بادی اولیه به منظور اتصال به آنتی ژن افزوده می شود. سپس آنتی بادی ثانویه که به صورت نشان دار شده است، افزوده می شود. مولکول بیوتین جهت اتصال استفاده می شود و پروب های فلوئورسنتی مانند فلوئورسئین و یا رودامین و کانژوگه های آنزیمی مانند HRP یا آلکالین فسفاتاز برای شناسایی و تولید سیگنال مورد استفاده قرار می گیرند. شکل زیر اصول کلی این دو نوع تکنیک ایمونوبلاتینگ را نشان می دهد.
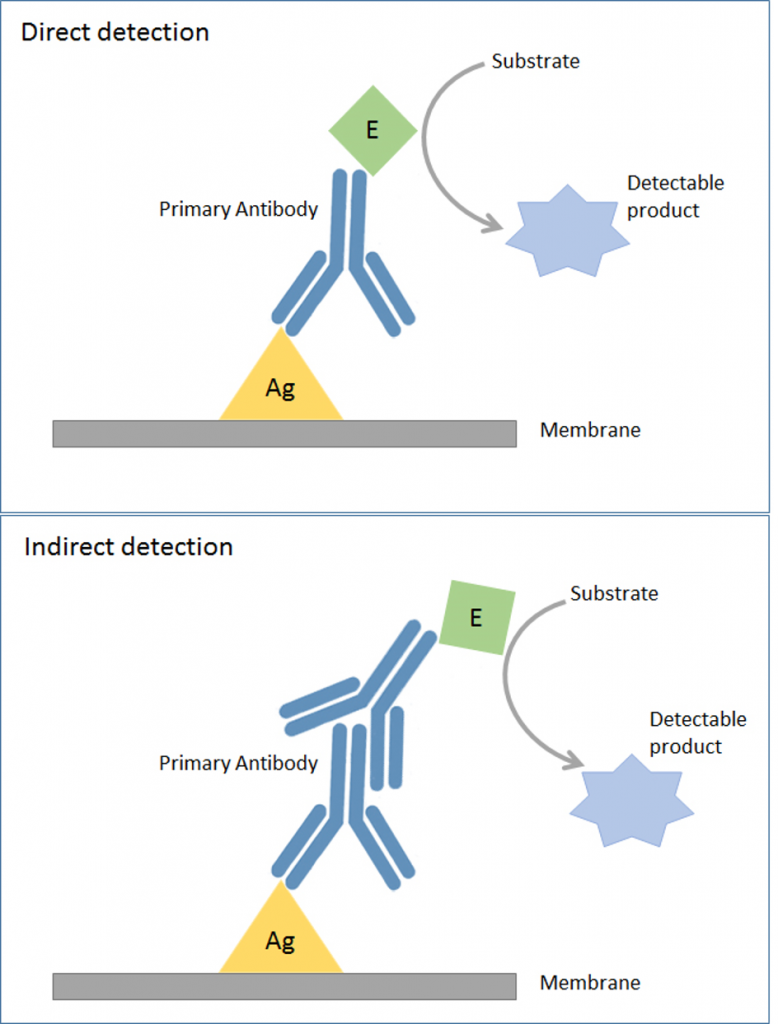
شکل ۸) روش های مختلف شناسایی با استفاده از آنتی بادی. در قسمت A به صورت مستقیم پروتئین هدف تشخیص داده می شود. در قسمت B به صورت غیر مستقیم مولکول هدف شناسایی می شود.
مواد
- بافر تریس نمکی با PH 7.5 (TBS). این بافر شامل تریس ۲۰ میلی مولار و کلرید سدیم ۱۵/۰ مولار است.
- بافر تریس نمکی حاوری توین ۰۵/۰ درصد (TBS-T). به هر لیتر از بافر تریس نمکی ۵/۰ میلی لیتر توین- ۲۰ اضافه شود.
- آنتی بادی اولیه (سرم بیمار یا حیوان ایمن شده). در صورت لزوم با TBS-T رقیق می گردد.
- آنتی بادی ثانویه . این آنتی بادی ضد بخش ثابت آنتی بادی اول است و با آنزیم (پراکسیداز) کونژوگه شده است. رقت مورد نیاز از این آنتی بادی در TBS-T تهیه می شود.
- محلول سوبسترای آنزیم پراکسیداز شامل دی آمینو بنزیدین ۵/۰ میلی گرم در میلی لیتر و پراکسید هیدروژن ۱/۰ درصد در TBS است.
روش آزمایش
- پس از مرحله مسدودسازی، غشا را ۳ بار، هربار ۵ دقیقه در TBS-T بشویید. سپس ۱-۲ ساعت در آنتی بادی اول قرار دهید.
- غشا را ۴ بار هر بار ۵ دقیقه در TBS-T بشویید. سپس ۱-۲ ساعت در آنتی بادی ثانویه (آنتی بادی کانژوگه با پراکسیداز) قرار دهید.
- غشا را ۴ بار هر بار ۵ دقیقه در TBS-T بشویید. سپس آن را در معرض مقدار کافی از محلول سوبسترا قرار دهید. ظهور باندها معمولا ۵-۱۵ دقیقه طول می کشد. پس از ظهور باندها غشا را در آب مقطر زیاد بشویید. غشا را خشک کرده، در محل تاریک قرار دهید.
توجه شود که دی آمینوبنزیدین یک ماده بسیار سمی است. از تماس با آن خودداری کنید و در استفاده از آن دقت نمایید.
| انتقال | |
| مسدود نمودن نواحی متصل نشده بر روی غشا | |
| انکوباسیون با آنتی بادی اولیه | |
| شستشو | |
| انکوباسیون با آنتی بادی ثانویه کانژوگه شده یا لیگاند | |
| شستشو | |
| ایجاد سیگنال بر اساس رنگ یا خاصیت لومینسانس | |
| مشاهده و عکس برداری با ژل داکیومنت و آنالیز نتایج |
جدول ۴) مراحل کلی فرایند وسترن بلات
فیلم آموزشی روش بلاتینگ نیمه خشک (سمی درای) | Semi-dry blotting
فیلم آموزشی روش بلاتینگ نیمه خشک (سمی درای) | Semi-dry blotting
♦♦♦ در صورت داشتن هرگونه سوال در مورد این موضوع برای ما نظر بگذارید (در پایین همین صفحه). در اسرع وقت به تمامی سوالات شما توسط کارشناس مربوطه پاسخ داده خواهد شد. با تشکر ♦♦♦
مطالب مشابه:
کامل ترین مجموعه کروماتوگرافی |انواع و روشهای کروماتوگرافی| بیوتکنولوژی
طراحی آزمایش چیست؟ | آموزش کلیات به همراه توضیحات کامل هر مرحله